题目内容
12.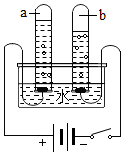 通电分解水的实验.回答问题:
通电分解水的实验.回答问题:(1)与正极相连的试管和与负极相连的试管中气体的体积比约为1:2.
(2)所发生化学反应方程式2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(3)该实验的结论是水是由氢元素和氧元素组成的.
分析 根据电解水的实验的现象及结论进行分析,记住口诀“正氧负氢,氢2氧1”.在电解水实验中,正极的气体体积少,能使带火星的木条复燃,是氧气;负极的气体体积多,能燃烧,是氢气,而且体积多的是少的二倍,该实验说明了水是由氢氧两种元素组成的.
解答 解:由电解水的实验的现象及结论可知:
(1)与正极相连的试管和与负极相连的试管中气体的体积比约为1:2;
(2)电解水的化学反应的化学反应方程式是:2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(3)通电分解水得到了氢气和氧气,该实验的结论是:水是由氢元素和氧元素组成的.
故答案为:
(1)1:2;(2)2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;(3)水是由氢元素和氧元素组成的.
点评 本题难度不大,考查学生对电解水实验的掌握情况,掌握电解水的实验现象、结论等是正确解答本题的关键.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
20.下列化学方程式书写没有错误的是( )
| A. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | B. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | ||
| C. | 2Al+O2═2AlO | D. | 2HgO $\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ |
7.如图所示实验操作正确的是( )
| A. |  过滤 | B. | 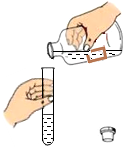 倾倒液体 | C. | 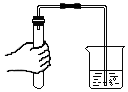 检查气密性 | D. | 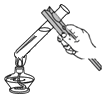 加热液体 |
1.根据化学方程式 4K2Cr2O7$\frac{\underline{\;灼烧\;}}{\;}$4K2CrO4+2R+3O2↑ 可推测R化学式是( )
| A. | CrO | B. | Cr2O3 | C. | CrO2 | D. | CrO3 |
2.下列化学方程式书写正确的是( )
| A. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | B. | 2Fe+6HCl═2FeCl2+3H2↑ | ||
| C. | KMnO4═K2MnO4+MnO2+O2 | D. | Fe+CuSO4═FeSO4+Cu↑ |
 干冰是固态的二氧化碳,在常温下易升华,如图是干冰升华时的情景,根据图中信息,从“物质性质决定反映物质用途”这一角度分析干冰具有的性质和用途.
干冰是固态的二氧化碳,在常温下易升华,如图是干冰升华时的情景,根据图中信息,从“物质性质决定反映物质用途”这一角度分析干冰具有的性质和用途.