题目内容
5.配平下列化学方程式.①1Fe+2HCl--1FeCl2+1H2
②1Fe2O3+3CO--2Fe+3CO2
③8Al+3Fe3O4--9Fe+4Al2O3
④1CH4+2O2--1CO2+2H2O
⑤5KClO3+6P--5KCl+3P2O5.
分析 根据质量守恒定律:反应前后各原子的数目不变,选择相应的配平方法(最小公倍数法、定一法等)进行配平即可;配平时要注意化学计量数必须加在化学式的前面,配平过程中不能改变化学式中的下标;配平后化学计量数必须为整数.
解答 解:①本题可利用“定一法”进行配平,把FeCl2的化学计量数定为1,则铁、盐酸、氢气前面的化学计量数分别为:1、2、1.
②本题可从得失氧的角度配平,一个CO分子反应中获得一个氧原子变为二氧化碳分子,由于一个Fe2O3分子中氧原子的数目为3个,所以CO与CO2前面的化学计量数都为3,最后配平其它元素的原子,Fe2O3、Fe前面的化学计量数分别为1、2.
③利用最小公倍数法进行配平,以氧原子作为配平的起点,四氧化三铁、氧化铝前面的化学计量数分别为:2、1,最后调整铝、铁前面的化学计量数为8、9.
④本题可利用“定一法”进行配平,把CH4的化学计量数定为1,则氧气、二氧化碳、水前面的化学计量数分别为:2、1、2.
⑤利用最小公倍数法进行配平,以氧原子作为配平的起点,氯酸钾、五氧化二磷前面的化学计量数分别为:2、1,最后调整磷、氯化钾前面的化学计量数为6、5.
故答案为:①1、2、1、1;②1、3、2、3;③8、3、9、4;④1、2、1、2;⑤5、6、5、3.
点评 本题难度不大,配平时化学计量数必须加在化学式的前面,配平过程中不能改变化学式中的下标;配平后化学计量数必须为整数,配平过程中若出现分数,必须把分数去分母转化为整数.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.有一包白色粉末可能由氯化钠、硫酸钠、硫酸铜、碳酸钠、碳酸钙中的一种或几种组成,为确定其组成,进行如下实验:
①称取一定质量的该白色粉末加足量水溶解,得无色溶液A;
②在无色溶液A中加入过量氯化钡溶液,充分反应后过滤,分别得无色溶液B和白色沉淀C;将白色沉淀C洗涤,烘干后称得质量为19g;
③在19g白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出;
④在无色溶液B中滴加硝酸银溶液和稀硝酸,产生白色沉淀;
根据上述实验现象判断,下列说法正确的是( )
①称取一定质量的该白色粉末加足量水溶解,得无色溶液A;
②在无色溶液A中加入过量氯化钡溶液,充分反应后过滤,分别得无色溶液B和白色沉淀C;将白色沉淀C洗涤,烘干后称得质量为19g;
③在19g白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出;
④在无色溶液B中滴加硝酸银溶液和稀硝酸,产生白色沉淀;
根据上述实验现象判断,下列说法正确的是( )
| A. | 白色粉末中不含碳酸钙、硫酸钠、硫酸铜 | |
| B. | 无色溶液B中一定含有两种溶质 | |
| C. | 白色粉末中一定含有氯化钠 | |
| D. | 步骤③生成的气体质量可能是4.4g |
6.如图所示装置有多种用途,下列说法错误的是( )


| A. | 洗气:除去CO中的HCl,装置内应盛H2O | |
| B. | 检验:证明CO中混有CO2,装置内应盛澄清石灰水 | |
| C. | 集气:若用排空气法收集比空气轻的气体时,气体应从装置的A端通入 | |
| D. | 若要测定实验室制得的少量02的体积,则应在瓶内先装满水,再将O2从B端通入 |
10.下列说法正确的是( )
| A. | 生成盐和水的反应都是中和反应;用烧碱可以改良酸性土壤 | |
| B. | 服用氢氧化钠治疗胃酸过多;干电池可以将电能转化为化学能 | |
| C. | 维生素不能提供能量所以对人体用处不大;硒是人体必须的微量元素,应大量服用 | |
| D. | 使用新能源,能减少酸雨产生;误食重金属盐,可立即服用蛋清或牛奶解毒 |
14.下列实验操作正确的是( )
| A. |  测溶液pH | B. |  过滤 | C. |  稀释浓硫酸 | D. |  检查气密性 检查气密性 |
 小佳同学取14%的硫酸溶液70g于烧杯中,然后向烧杯中慢慢加入10g氧化铜粉末并不断搅拌,测得烧杯中溶液的质量与加入氧化铜粉末的质量关系如图所示
小佳同学取14%的硫酸溶液70g于烧杯中,然后向烧杯中慢慢加入10g氧化铜粉末并不断搅拌,测得烧杯中溶液的质量与加入氧化铜粉末的质量关系如图所示

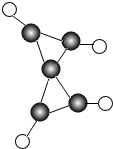 通过化学的学习,小明同学感悟到学习化学开拓了思维、增长了智慧.
通过化学的学习,小明同学感悟到学习化学开拓了思维、增长了智慧. ”代表碳原子,“
”代表碳原子,“ ”代表氢原子.请补充该物质燃烧的化学方程式:C5H4+6O2 $\frac{\underline{\;点燃\;}}{\;}$5CO2+2H2O.
”代表氢原子.请补充该物质燃烧的化学方程式:C5H4+6O2 $\frac{\underline{\;点燃\;}}{\;}$5CO2+2H2O.