题目内容
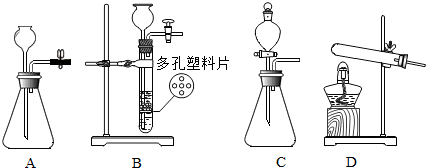
11.下列实验操作,不正确或不能达到实验目的是( )| A. |  读液体体积 | B. |  验证质量守恒定律 | ||
| C. |  测溶液的pH | D. |  稀释浓硫酸 |
分析 A、根据量筒的读数注意事项进行分析;
B、做验证质量守恒定律的实验时所选用的装置应该考虑到:如果反应物中有气体参加反应,或生成物中有气体生成,应该选用密闭装置;
C、用pH试纸测定液体的酸碱度时,要用滴管或玻璃棒将液体滴加到干燥的试纸上;
D、运用稀释浓硫酸时不能将水倒入浓硫酸中,要将浓硫酸倒入水中进行分析;
解答 解:A、利用量筒量取液体时,读数时视线要与凹液面的最低处保持相平,故A正确;
B、验证质量守恒定律时,有气体生成或参加的需放在密闭容器内进行,不然不能达到目的,故B错误;
C、用pH试纸测定液体的酸碱度时,要用滴管或玻璃棒将液体滴加到干燥的试纸上,故C正确;
D、稀释浓硫酸时不能将水倒入浓硫酸中要将浓硫酸倒入水中,防止水浮在浓硫酸的水面上沸腾溅出,要将浓硫酸慢慢注入水中,并不断搅拌,故D正确;
故选B.
点评 本题考察了实验基本技能,实验基本操作,所以要求同学们在平时的学习中加强基础知识的记忆,以便能够灵活应用.

练习册系列答案
相关题目
1.下列鉴别物质的试剂或方法,不正确的是( )
| A. | 用氯化钡区分稀盐酸和稀硫酸 | |
| B. | 用紫色石蕊溶液区分二氧化碳和一氧化碳 | |
| C. | 用水区分硝酸铵固体和氢氧化钠固体 | |
| D. | 用二氧化碳区分氯化钠溶液和氢氧化钠溶液 |
6.将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)$\stackrel{O_{2}}{→}$ 钠的氧化物 $\stackrel{H_{2}O}{→}$ 氢氧化钠溶液 $\stackrel{CO_{2}}{→}$ 白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH; 2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O 猜想2:Na2O2 猜想3:Na2O和Na2O2
【实验探究一】:
【继续探究】:钠在空气中放置一段时间得到白色固体的成分
【作出猜想】猜想一:Na2CO3猜想二:Na2CO3和NaOH
【实验探究二】:
【实验反思】
(1)类比氧化铁与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl═4NaCl+2H2O+X,X的化学式为O2.
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).
钠(Na)$\stackrel{O_{2}}{→}$ 钠的氧化物 $\stackrel{H_{2}O}{→}$ 氢氧化钠溶液 $\stackrel{CO_{2}}{→}$ 白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH; 2Na2O2+2H2O═4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O 猜想2:Na2O2 猜想3:Na2O和Na2O2
【实验探究一】:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 无气泡生成 | 猜想1正确 |
【作出猜想】猜想一:Na2CO3猜想二:Na2CO3和NaOH
【实验探究二】:
| 实验操作 | 实验现象 | 实验结论 |
| 1、取少量白色固体加入足量CaCl2溶液. | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2、过滤、取少量滤液加入 无色酚酞试液 | 试液变红 |
(1)类比氧化铁与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl═4NaCl+2H2O+X,X的化学式为O2.
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).
16.有元素化合价升降的反应属于氧化还原反应,下列不属于氧化还原反应的是( )
| A. | NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+CO2↑+H2O | B. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | ||
| C. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | D. | 2Na2O2+2H2O═4NaOH+O2↑ |
20.下列过程属于化学变化的是( )
| A. | 甲烷燃烧 | B. | 干冰升华 | C. | 汽油挥发 | D. | 西瓜榨汁 |
1.化学实验室常需要配制溶液,下列说法正确的是( )
| A. | 配制溶液时,只能用水作溶剂 | |
| B. | 配制硝酸铵溶液的过程中,溶液的温度会下降 | |
| C. | 用浓硫酸配制稀硫酸时,应将水缓缓注入浓硫酸中 | |
| D. | 将10g氯化钠溶于100g水中,得到质量分数为10%的氯化钠溶液 |