题目内容
已知用10%氢氧化钾溶液56g滴加到18.5g稀盐酸中(含2滴酚酞试液),混合液刚好由无色变为粉红色时,可认为恰好完全反应.
(1)求算反应后所得溶液的溶质质量分数.
(2)试列式计算说明将该反应后所得溶液冷却室温20℃,要配制此温度时的饱和溶液最简单的方法是 (计算结果精确到0.1g).已知:20℃时氯化钾的溶解度为34g.

(1)求算反应后所得溶液的溶质质量分数.
(2)试列式计算说明将该反应后所得溶液冷却室温20℃,要配制此温度时的饱和溶液最简单的方法是
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)依据反应的情况结合化学方程式的计算,对反应后所得溶液的溶质质量分数进行计算即可;
②根据20℃是氯化钾的溶解度,结合溶液中含有的氯化钾质量分析使其转化为20℃时的饱和溶液的方法.
②根据20℃是氯化钾的溶解度,结合溶液中含有的氯化钾质量分析使其转化为20℃时的饱和溶液的方法.
解答:解:(1)由题干可知10.0%的氢氧化钾溶液56.0g和18.5g盐酸恰好完全反应,可计算出生成的氯化钾质量;
设,生成的氯化钾的质量是x.
K0H+HCl═KCl+H2O
56 74.5
56g×10% x
=
x=7.45g
反应后所得溶液的溶质质量分数:
×100%=10%,
(2)由于该溶液在20℃时不饱和所以可采用加溶质的简便办法使其转化成饱和溶液,原溶液质量是20g+16g=36g;
设加入溶质的质量是y,则有
×100%=
×100%,
y=15.3g
答:(1)反应后所得溶液的溶质质量分数10%;
(2)加氯化钾 15.3g.
设,生成的氯化钾的质量是x.
K0H+HCl═KCl+H2O
56 74.5
56g×10% x
| 56 |
| 56g×10% |
| 74.5 |
| x |
x=7.45g
反应后所得溶液的溶质质量分数:
| 7.45g |
| 56g+18.5g |
(2)由于该溶液在20℃时不饱和所以可采用加溶质的简便办法使其转化成饱和溶液,原溶液质量是20g+16g=36g;
设加入溶质的质量是y,则有
| 34g |
| 100g+34g |
| 7.45g+y |
| 74.5g+y |
y=15.3g
答:(1)反应后所得溶液的溶质质量分数10%;
(2)加氯化钾 15.3g.
点评:此题是一道计算综合题,解题的关键是充分利用题干中提供的新信息并结合相关的基础计算完成,题型涉及面广起点较高但落点较低.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列厨房中常见的操作或现象,其中涉及化学变化的是( )
| A、水果榨汁 | B、萝卜剁碎 |
| C、铁锅生锈 | D、汤中加盐 |
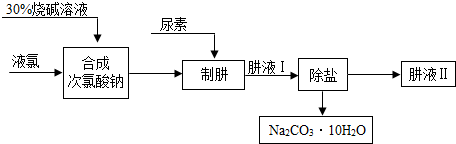
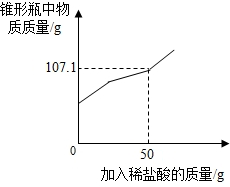 某兴趣小组在实验室发现一瓶敞口久置的氢氧化钠和一瓶未标浓度的稀盐酸,为测定氢氧化钠的变质情况和稀盐酸的浓度,他们取9.3g变质的氢氧化钠样品于锥形瓶中,加入50g水,充分溶解,再向锥形瓶中滴加未知浓度的稀盐酸,实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如图所示.
某兴趣小组在实验室发现一瓶敞口久置的氢氧化钠和一瓶未标浓度的稀盐酸,为测定氢氧化钠的变质情况和稀盐酸的浓度,他们取9.3g变质的氢氧化钠样品于锥形瓶中,加入50g水,充分溶解,再向锥形瓶中滴加未知浓度的稀盐酸,实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如图所示.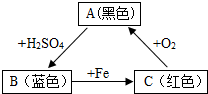 A、B、C三种物质(或溶液)可发生如图所示的转化.
A、B、C三种物质(或溶液)可发生如图所示的转化.