题目内容
9.小刚同学在实验室中用一种紫褐色固体粉末A进行探究实验,他实验的过程和现象如下,请你帮其解决下列问题:
(1)写出下列物质的化学式:A:KMnO4 B:O2 F:H2O2.
(2)反应①的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应的基本反应类型为:分解.
(3)反应③的主要实验现象是:火星四射,放出大量热,生成黑色固体,
化学方程式:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,反应基本类型为:化合反应.
分析 本题的突破口是紫褐色粉末和反应③条件,根据无色气体B和铁丝燃烧生成固体E,可以推测B是氧气、固体E是四氧化三铁;根据反应①②和氧气的实验室制法可知,A是高锰酸钾、C是二氧化锰、F是过氧化氢.据此完成相关的问题即可.
解答 解:(1)根据物质颜色和重要的化学反应,可以推测各种物质的名称;无色气体B和铁丝燃烧生成固体E,可以推测B是氧气、固体E是四氧化三铁;根据反应①②和氧气的实验室制法可知,A是高锰酸钾、B是单质氧气,C是二氧化锰、F是过氧化氢.故答案为:KMnO4; O2; H2O2.
(2)反应①为高锰酸钾分解产生锰酸钾、二氧化锰和氧气,是一种物质生成三种物质的分解反应,故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;分解;
(3)铁和氧气燃烧生成四氧化三铁,反应的现象为:火星四射,放出大量热,生成黑色固体;该反应是两种或者两种以上物质生成一种物质的反应,属于化合反应.故答案为:火星四射,放出大量热,生成黑色固体;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;化合.
故答案为:
(1)KMnO4; O2;H2O2.
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,分解.
(3)火星四射,放出大量热,生成黑色固体,3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,化合.
点评 本题属于常见物质的推断题,在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.

练习册系列答案
相关题目
19.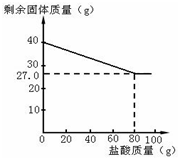 某化学兴趣小组的同学为测定假黄金(铜锌合金)中各组成元素的质量分数,称取40克假黄金置于烧杯中,用某浓度的稀盐酸100克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:
某化学兴趣小组的同学为测定假黄金(铜锌合金)中各组成元素的质量分数,称取40克假黄金置于烧杯中,用某浓度的稀盐酸100克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:
(1)从图可知,当所用合金与稀盐酸的质量比为1:2时,表明锌恰好完全反应.
(2)求铜锌合金中锌的质量分数;
(3)计算稀盐酸中溶质的质量分数.
 某化学兴趣小组的同学为测定假黄金(铜锌合金)中各组成元素的质量分数,称取40克假黄金置于烧杯中,用某浓度的稀盐酸100克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:
某化学兴趣小组的同学为测定假黄金(铜锌合金)中各组成元素的质量分数,称取40克假黄金置于烧杯中,用某浓度的稀盐酸100克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:| 实验次数 | 稀盐酸的用量(g) | 剩余固体的质量(g) |
| 1 | 20 | 36.75 |
| 2 | 20 | 33.50 |
| 3 | 20 | 30.25 |
| 4 | 20 | 27.00 |
| 5 | 20 | 27.00 |
(2)求铜锌合金中锌的质量分数;
(3)计算稀盐酸中溶质的质量分数.
17.硫酸、盐酸、硝酸都是常见的酸,我们之所以认为它们是酸,最根本的原因是( )
| A. | 它们的pH小于7 | B. | 它们电离时产生的阳离子只有H+ | ||
| C. | 它们遇紫色石蕊变红色 | D. | 它们有酸味 |
4.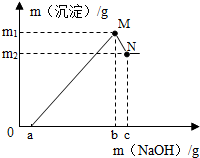 已知:MgSO4+2NaOH═Mg(OH)2↓+Na2SO4,Al2(SO4)3+6NaOH═2Al(OH)3↓+3Na2SO4,Al(OH)3+NaOH═NaAlO2+2H2O,Mg(OH)2不溶于NaOH溶液.现剪取wg镁铝合金的易拉罐壳,先用过量硫酸溶解,然后再向溶液中滴加NaOH溶液,反应符合如图关系(横坐标表示滴加NaOH溶液的质量,纵坐标表示生成沉淀的质量),则下列说法不正确的是( )
已知:MgSO4+2NaOH═Mg(OH)2↓+Na2SO4,Al2(SO4)3+6NaOH═2Al(OH)3↓+3Na2SO4,Al(OH)3+NaOH═NaAlO2+2H2O,Mg(OH)2不溶于NaOH溶液.现剪取wg镁铝合金的易拉罐壳,先用过量硫酸溶解,然后再向溶液中滴加NaOH溶液,反应符合如图关系(横坐标表示滴加NaOH溶液的质量,纵坐标表示生成沉淀的质量),则下列说法不正确的是( )
 已知:MgSO4+2NaOH═Mg(OH)2↓+Na2SO4,Al2(SO4)3+6NaOH═2Al(OH)3↓+3Na2SO4,Al(OH)3+NaOH═NaAlO2+2H2O,Mg(OH)2不溶于NaOH溶液.现剪取wg镁铝合金的易拉罐壳,先用过量硫酸溶解,然后再向溶液中滴加NaOH溶液,反应符合如图关系(横坐标表示滴加NaOH溶液的质量,纵坐标表示生成沉淀的质量),则下列说法不正确的是( )
已知:MgSO4+2NaOH═Mg(OH)2↓+Na2SO4,Al2(SO4)3+6NaOH═2Al(OH)3↓+3Na2SO4,Al(OH)3+NaOH═NaAlO2+2H2O,Mg(OH)2不溶于NaOH溶液.现剪取wg镁铝合金的易拉罐壳,先用过量硫酸溶解,然后再向溶液中滴加NaOH溶液,反应符合如图关系(横坐标表示滴加NaOH溶液的质量,纵坐标表示生成沉淀的质量),则下列说法不正确的是( )| A. | a点表示NaOH溶液与剩余的硫酸恰好完全反应 | |
| B. | 在M点时,溶液中只有一种溶质 | |
| C. | N点表示Al(OH)3沉淀刚好完全溶于NaOH溶液 | |
| D. | 生成Mg(OH)2沉淀的质量为(m1+m2)g |
14.到高中我们将从元素原子得失电子的角度来认识氧化还原反应,而元素原子得失电子表现为元素化合价的变化.因此可以把元素化合价有升降的化学反应确定为氧化还原反应,据此可判断下列化学反应属于氧化还原的是( )
| A. | Zn(OH)2+2HClO4═Zn(ClO4)2+2H2O | B. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | ||
| C. | Fe3O4+4H2$\frac{\underline{\;高温\;}}{\;}$3Fe+4H2O | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ |
1.铈(Ce)是一种常见的稀土元素,铈元素的原子序数是58,下列关于铈的说法正确的是( )
| A. | 相对原子质量为58 | B. | 中子数为58 | ||
| C. | 相对原子质量为140.1g | D. | 质子数为58 |