题目内容
6.实验室用50g质量分数为14.6%的稀盐酸与足量的石灰石反应制取二氧化碳,计算生成二氧化碳的质量是多少克?分析 根据消耗的HCl的质量和对应的化学方程式求算生成的二氧化碳.
解答 解:消耗的HCl的质量为50g×14.6%=7.3g
设生成二氧化碳的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 44
7.3g x
$\frac{73}{44}$=$\frac{7.3g}{x}$
x=4.4g
答:生成二氧化碳的质量是4.4g.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
17.下列符号中既表示一种元素,又表示一个原子,还能表示一种单质的是( )
| A. | O | B. | O2 | C. | 2O2 | D. | Fe |
14.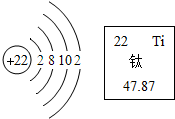 钛被称为“21世纪金属”.如图是钛的原子结构示意图和在元素周期表中的信息,下列有关钛的说法错误的是( )
钛被称为“21世纪金属”.如图是钛的原子结构示意图和在元素周期表中的信息,下列有关钛的说法错误的是( )
 钛被称为“21世纪金属”.如图是钛的原子结构示意图和在元素周期表中的信息,下列有关钛的说法错误的是( )
钛被称为“21世纪金属”.如图是钛的原子结构示意图和在元素周期表中的信息,下列有关钛的说法错误的是( )| A. | 属于金属元素 | B. | 核电荷数是22 | ||
| C. | 钛原子有4个电子层 | D. | 钛原子易形成阴离子 |
11.区分下列各组物质的两种方法都合理的是( )
| 选项 | 需区分的物质 | 方法一 | 方法二 |
| A | 硬水和软水 | 分别加入肥皂水 | 蒸干比较固体的多少 |
| B | 硝酸铵和尿素 | 加碱研磨,闻气味 | 溶于水,看是否吸热 |
| C | 黄金和黄铜 | 加入硫酸锌溶液 | 在空气中加热 |
| D | 二氧化碳和氮气 | 分别通入澄清的石灰水 | 分别伸入燃烧的木条 |
| A. | A | B. | B | C. | C | D. | D |
18.有利于保护环境的是( )
| A. |  随意扔垃圾 | B. |  废水排入河流 | ||
| C. |  金属回收再利用 | D. |  废气排到高空 |