题目内容
12.钛和钛合金被称为“未来的金属材料”.(1)工业上以金红石(主要成分是TiO2)为原料生产金属钛,其工艺流程如下:

①可燃性气体X的化学式是一氧化碳;
②化学反应Ⅱ的化学方程式为TiCl4+2Mg=2MgCl2+Ti.
(2)Ti、Al、Cu三种金属在稀盐酸里的反应现象如图所示,由图可知Y所代表的金属是铜.

分析 (1)根据化学反应前后元素种类守恒和常见的可燃性气体解答;根据四氯化钛和镁反应生成氯化镁和钛解答;
(2)根据Y的表面没有气泡分析Y金属.
解答 解:(1)①碳、二氧化钛和氯气反应生成四氯化钛和可燃性气体X,所有X中含有碳、氧元素,一氧化碳具有可燃性,故答案:一氧化碳;
②四氯化钛和镁反应生成氯化镁和钛,故答案:TiCl4+2Mg=2MgCl2+Ti;
(2)由于Y的表面没有气泡生成,说明了Y不能与酸反应,故Y为铜;故填:铜.
点评 本题考查物质的化学性质,注重对信息处理和利用能力的考查.

练习册系列答案
相关题目
11. 某科学兴趣小组为了测定实验室中久置的NaOH的变质程度,进行了下列实验,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.则下列针对本实验的说法中错误的是( )
某科学兴趣小组为了测定实验室中久置的NaOH的变质程度,进行了下列实验,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.则下列针对本实验的说法中错误的是( )
 某科学兴趣小组为了测定实验室中久置的NaOH的变质程度,进行了下列实验,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.则下列针对本实验的说法中错误的是( )
某科学兴趣小组为了测定实验室中久置的NaOH的变质程度,进行了下列实验,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.则下列针对本实验的说法中错误的是( )| A. | 产生CO2气体的质量为2.2g | B. | Na2CO3的质量为5.3g | ||
| C. | 变质的NaOH的质量为4.0g | D. | NaOH的变质程度为30% |
9.取一定量的氧化镁与氧化铜的混合物,向其中加入溶质质量分数为14.6%的稀盐酸100g,恰好完全反应生成盐和水.则原混合物中氧元素的质量是( )
| A. | 14.6g | B. | 3.6g | C. | 3.2g | D. | 1.4g |
7. 如图所示,广口瓶内加入了一定量的固体,将胶头滴管中的液体滴加到广口瓶中的固体上,不能使b端液面明显卡簧的固体和液体组合是( )
如图所示,广口瓶内加入了一定量的固体,将胶头滴管中的液体滴加到广口瓶中的固体上,不能使b端液面明显卡簧的固体和液体组合是( )
 如图所示,广口瓶内加入了一定量的固体,将胶头滴管中的液体滴加到广口瓶中的固体上,不能使b端液面明显卡簧的固体和液体组合是( )
如图所示,广口瓶内加入了一定量的固体,将胶头滴管中的液体滴加到广口瓶中的固体上,不能使b端液面明显卡簧的固体和液体组合是( )| A. | 锌粒和稀硫酸 | B. | 氢氧化钠固体和水 | ||
| C. | 生石灰固体和水 | D. | 硝酸铵固体和水 |
17.下列原子结构示意图中,表示稀有气体元素原子的是( )
| A. | 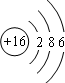 | B. | 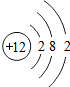 | C. | 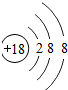 | D. | 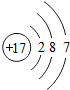 |
4.若用“ ”表示氢原子,下列方框中能表示2H2的意义的是( )
”表示氢原子,下列方框中能表示2H2的意义的是( )
 ”表示氢原子,下列方框中能表示2H2的意义的是( )
”表示氢原子,下列方框中能表示2H2的意义的是( )| A. |  | B. | 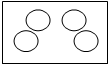 | C. | 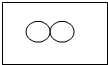 | D. | 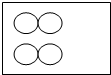 |
1.取一个大萝卜,中间挖一个孔制成杯状,向其中注入一定量的饱和食盐水,过一段时间后将孔里的食盐水倒出,下列说法正确的是( )
| A. | 倒出仍是饱和食盐水 | B. | 倒出溶液的溶质质量分数变小了 | ||
| C. | 倒出溶液的溶解度变小 | D. | 倒出溶液的溶质质量分数变大了 |