题目内容
16.将铁片分别投入下列溶液中,溶液的质量会减少的是( )| A. | 硫酸铜 | B. | 稀硫酸 | C. | 硫酸亚铁 | D. | 稀盐酸 |
分析 根据金属活动性顺序及各物质发生化学反应时的质量比进行分析解答.在金属活动性顺序表中,氢前面的金属能和常见的酸反生反应置,位于前面的金属能把排在它后面的金属从其盐溶液中转换出来.首先确定把铁加入溶液中是否发生反应,如果不反应,则溶液的质量保持不变;如果反应,再看反应后生成的溶质的质量是否增大或减小,从而判断出溶液的质量的变化.
解答 解:A、把铁片放入硫酸铜溶液中,铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,由反应时的质量比可知,每56份质量的铁可置换出64份质量的铜,溶液的质量会减少,故A正确;
B、铁与稀硫酸能反应,生成氢气和硫酸亚铁而使溶液质量增加,其原因是:由反应的化学方程式:Fe+H2SO4=FeSO4+H2↑,可知56gFe反应溶液增加(56-2)=54g,所以溶液质量增加,故B错误;
C、铁与硫酸亚铁不能反应,所以溶液质量不会变化,故C错误;
D、铁与稀盐酸能反应,生成氢气和氯化亚铁而使溶液质量增加,其原因是:由反应的化学方程式:Fe+2HCl═FeCl2+H2↑,可知56gFe反应溶液增加(56-2)=54g,所以溶液质量增加,故D错误.
故选:A.
点评 本题难度不是很大,掌握金属的活动性顺序表及其应用并能结合质量守恒定律判断溶液质量的变化情况是正确解答本题的关键.

练习册系列答案
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
3.下列化学用语与含义不相符的是( )
| A. | S2--硫离子 | B. | 3O-3个氧元素 | C. | Fe2O3-氧化铁 | D. | 2H2-2个氢气分子 |
4.下列有关资源、能源的叙述,不正确的是( )
| A. | 使用清洁能源、植树造林等可以更好地保护空气,防止雾霾 | |
| B. | 爱护水资源一方面要节约用水,另一方面要防止水体污染 | |
| C. | 防锈、回收、合理开采是保护金属资源的有效措施 | |
| D. | 天然气是较为清洁的可再生能源 |
4.有甲、乙、丙、丁四种金属,将它们分别投入到相同的稀盐酸中,只有丙、丁的表面有气泡产生,且丙产生的气泡比丁快;再将乙投入到甲的盐溶液中,乙的表面有甲析出,则四种金属的活动性顺序正确的是( )
| A. | 丙>丁>乙>甲 | B. | 甲>乙>丙>丁 | C. | 丙>丁>甲>乙 | D. | 无法判断 |
1.化学是一门研究物质的科学,我们一般从物质的存在、性质、制备、用途等方面研究一种物质或一类物质.以金属为例,请你参与其中回答相关问题:
(1)认识金属元素存在:自然界中大多数金属都以化合物的形式存在.下列矿石的主要成分属于氧化物的是AD(填字母序号,下同);
A.铝土矿 (主要成分A1203) B.辉铜矿(主要成分Cu2S)
C.菱铁矿 (主要成分FeC03) D.磁铁矿 (主要成分Fe304)
(2)探究金属物理性质:
如表是A、B、C三种金属的部分物理性质.
①高压输电线不用金属A而选用金属B,主要原因是电性较好、密度小.
②C的合金通常可以做菜刀、锤子等,其合金的硬度>5(填“>”“<”或“=”).
(3)探究金属化学性质:金属原子容易失去最外层电子,化学性质活泼.
材料:我国第四套人民币中的一元硬币是钢芯镀镍(Ni),镍与稀硫酸能发生下列反应:
Ni+H2SO4═NiSO4+H2↑.
写出Ni与CuSO4溶液发生置换反应的方程式Ni+CuSO4═Cu+NiSO4.
(4 )认识金属的制备:工业上常采用还原法、置换法、电解法制备金属.
用一氧化碳还原赤铁矿冶铁反应的化学方程式为_Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 .
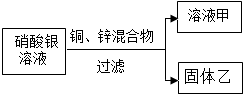
(5)金属在生产生活中应用广泛.如图,向一定量硝酸银溶液中加入铜和锌的混合粉末,充分反应后过滤,得溶液甲和固体乙.
①若乙中含有锌、铜、银三种固体,此时向固体乙中加入稀盐酸,发生反应的化学方程式为Zn+2HCl=ZnCl2+H2↑.
②若溶液甲显蓝色,是因为Cu+2AgNO3═2Ag+Cu(NO3)2(用化学反应方程式表示),此时固体乙中一定含有的物质是银.
(1)认识金属元素存在:自然界中大多数金属都以化合物的形式存在.下列矿石的主要成分属于氧化物的是AD(填字母序号,下同);
A.铝土矿 (主要成分A1203) B.辉铜矿(主要成分Cu2S)
C.菱铁矿 (主要成分FeC03) D.磁铁矿 (主要成分Fe304)
(2)探究金属物理性质:
如表是A、B、C三种金属的部分物理性质.
| 性质 金属 | 导电性(100为标准) | 密度(g/cm3) | 熔点(℃) | 硬度(10为标准) |
| A | 99 | 8.92 | 1083 | 3 |
| B | 61 | 2.70 | 660 | 2.9 |
| C | 17 | 7.86 | 1535 | 5 |
②C的合金通常可以做菜刀、锤子等,其合金的硬度>5(填“>”“<”或“=”).
(3)探究金属化学性质:金属原子容易失去最外层电子,化学性质活泼.
材料:我国第四套人民币中的一元硬币是钢芯镀镍(Ni),镍与稀硫酸能发生下列反应:
Ni+H2SO4═NiSO4+H2↑.
写出Ni与CuSO4溶液发生置换反应的方程式Ni+CuSO4═Cu+NiSO4.
(4 )认识金属的制备:工业上常采用还原法、置换法、电解法制备金属.
用一氧化碳还原赤铁矿冶铁反应的化学方程式为_Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 .
(5)金属在生产生活中应用广泛.如图,向一定量硝酸银溶液中加入铜和锌的混合粉末,充分反应后过滤,得溶液甲和固体乙.

①若乙中含有锌、铜、银三种固体,此时向固体乙中加入稀盐酸,发生反应的化学方程式为Zn+2HCl=ZnCl2+H2↑.
②若溶液甲显蓝色,是因为Cu+2AgNO3═2Ag+Cu(NO3)2(用化学反应方程式表示),此时固体乙中一定含有的物质是银.
5.亮亮做家务时接触到下列用品.
(1)他清理垃圾时发现一袋脱氧剂,拆开后看到还原铁粉已生锈,铁生锈的原因是Fe与潮湿的空气接触.
(2)他选用洁厕灵清除水垢(主要成分是碳酸钙),用化学方程式表示其原理CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
(4)做完家务,他用Vc泡腾片冲了一杯饮料.下列Vc泡腾片的主要成分中,属于有机物的是AB(填字母序号).
A.维生素C(C6H8O6) B.柠檬酸(C6H8O7) C.碳酸氢钠(NaHCO3)
| 用品 | 脱氧剂 | 洁厕灵 | 炉灶清洁剂 |
| 有效成分 | 还原铁粉 | 盐酸 | 氢氧化钠 |
(2)他选用洁厕灵清除水垢(主要成分是碳酸钙),用化学方程式表示其原理CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是NaOH有强腐蚀性.
(4)做完家务,他用Vc泡腾片冲了一杯饮料.下列Vc泡腾片的主要成分中,属于有机物的是AB(填字母序号).
A.维生素C(C6H8O6) B.柠檬酸(C6H8O7) C.碳酸氢钠(NaHCO3)
6. 现有等质量的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价).则下列说法中正确的是( )
现有等质量的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价).则下列说法中正确的是( )
 现有等质量的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价).则下列说法中正确的是( )
现有等质量的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价).则下列说法中正确的是( )| A. | 相对原子质量:丙>乙>甲 | B. | 生成氢气的质量:丙>乙>甲 | ||
| C. | 所得溶液的质量:乙>甲>丙 | D. | 消耗硫酸的质量:丙>乙>甲 |