题目内容
8.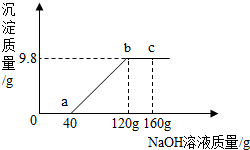 向只含CuCl2、HCl二种溶质的溶液50g加入NaOH溶液,产生沉淀的图示如图所示:
向只含CuCl2、HCl二种溶质的溶液50g加入NaOH溶液,产生沉淀的图示如图所示:(1)加40gNaOH溶液时不产生沉淀的化学方程式NaOH+HCl=NaCl+H2O.
(2)C点时对应的溶质NaCl、NaOH.
(3)求NaOH溶液中溶质的质量分数.
(4)根据如图和题意可求出的数据有A.
A.50g溶液中CuCl2与HCl的质量
B.C点中溶质的质量
C.b点溶液中溶质的质量分数
D.50g溶液中氢元素的质量分数.
分析 (1)加40gNaOH溶液时,氢氧化钠与稀盐酸发生中和反应;
(2)根据氢氧化钠与盐酸反应生成氯化钠和水,氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,还需要结合c点时氢氧化钠过量进行分析;
(3)根据沉淀质量计算出与氯化铜反应的氢氧化钠的质量,再除以氢氧化钠溶液的质量,求出溶质质量分数;
(4)根据如图和题意可求出的数据即可.
解答 解:(1)氢氧化钠与盐酸反应生成氯化钠和水,无沉淀生成;故填:NaOH+HCl=NaCl+H2O;
(2)氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,所以反应后溶液中的溶质一定含有氯化钠,c点时氢氧化钠过量,所以溶质中还含有氢氧化钠;
故填:NaCl、NaOH;
(3)设生成9.8g沉淀需要参加反应的氯化铜的质量为x,参加反应的氢氧化钠的质量为y则:
CuCl2+2NaOH═Cu(OH)2↓+2NaCl,
80 98
y 9.8g
根据:$\frac{80}{y}=\frac{98}{9.8g}$,
解得y=8g,
所以NaOH溶液中溶质的质量分数$\frac{8g}{120g-40g}$×100%=10%;
(4)由沉淀的质量可以求出NaOH溶液中溶质的质量分数,进而求出盐酸的质量,故选A.
故答案为:(1)NaOH+HCl=NaCl+H2O;(2)NaCl、NaOH;(3)10%;(4)A.
点评 本题考查化学方程式与溶液的综合计算,解题关键是分析清楚反应过程的先后,找出每个过程中已知物质的质量.要知道加入的氢氧化钠先与盐酸反应,把盐酸反应完了再与氯化铜反应.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
18.下列制备物质的设计中,理论上正确、操作上可行、经济上合理的是( )
| A. | CO$→_{△}^{CuO}$CO2$→_{溶液}^{NaOH}$Na2CO3溶液 | |
| B. | Cu$→_{溶液}^{AgNO_{3}}$ Cu(NO3)2溶液$→_{溶液}^{NaOH}$Cu(OH)2 | |
| C. | Fe$→_{点燃}^{O_{2}}$Fe2O3$\stackrel{稀硫酸}{→}$Fe2(SO4)3溶液 | |
| D. | CaO$\stackrel{H_{2}O}{→}$Ca(OH)2溶液$→_{溶液}^{Na_{2}CO_{3}}$ NaOH溶液 |
19.在一定温度下,某物质的饱和溶液一定( )
| A. | 是很浓的溶液 | B. | 含100g水的溶液 | ||
| C. | 不能再溶解该物质的溶液 | D. | 含100g该物质的溶液 |
13.2013年3月22日是第二十一届“世界水日”,3月22日至3月28日是第二十六届“中国水周”.我国确定“中国水周”宣传主题是“节约保护水资源,大力建设生态文明”.下列说法不符合该主题的是( )
| A. | 养成用水后随手关水龙头的习惯 | B. | 将死猪丢到江河中有利于鱼虾生长 | ||
| C. | 大力宣传使用节水马桶 | D. | 严禁工业污水任意排放 |
20.以下所列食物中富含蛋白质的是( )
| A. | 米饭 | B. | 菠菜 | C. | 肥肉 | D. | 鸡蛋 |
15.将CO2通入滴有酚酞的BaCl2、NaOH混合溶液中,出现白色沉淀.下列说法错误的是( )
| A. | 溶液的红色逐渐变浅或变为无色 | |
| B. | 反应后的溶液中一定有NaCl | |
| C. | 反应过程中,溶液里BaCl2、NaOH的质量分数均减小 | |
| D. | 产生白色沉淀的化学方程式为:BaCl2+CO2+H2O=BaCO3↓+2HCl |