题目内容
13. 如图是某种化肥标签上的部分说明.
如图是某种化肥标签上的部分说明.(1)取5L这种农用氨水稀释成可供施用的稀氨水,需要加水295.5kg.
(2)请用一种简单方法证明氨水呈碱性.(写出简单操作)
(3)根据氨水保存时的注意事项,试推测该物质具有的性质.
分析 (1)根据溶液稀释过程中,溶质的质量不变来分析;
(2)根据证明氨水显碱性可用酸碱指示剂进行解答;
(3)依据标签上的注意事项完成即可.
解答 解:(1)稀释过程中,溶质的质量不变,设需要加入水的质量为x,则
5L×0.90kg/L×20%=(5L×0.90kg/L+x)×0.3%
x=295.5kg
故填:295.5;
(2)证明氨水显碱性可用酸碱指示剂,例如石蕊或酚酞试液;故填:取少量氨水于试管中,然后滴加几滴无色酚酞试液,若观察到无色溶液变红色,则证明氨水显碱性(答案合理即可);
(3)根据使用注意事项中提示要密封保存、避光,可推断氨水易挥发、见光易分解等,故填:易挥发、见光易分解.
点评 本题考查了溶液的稀释、物质的检验等,掌握基本化学知识就能顺利解答.

练习册系列答案
相关题目
3.比较推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 金刚石和石墨都是碳的单质,金刚石很硬,故石墨也很硬 | |
| B. | 合金比组成它的纯金属硬,故黄铜比纯铜硬 | |
| C. | 稀硫酸能和氯化钡反应生成白色沉淀,故稀盐酸也可以 | |
| D. | 氢氧化镁和氢氧化钠都是碱,氢氧化镁可以治疗胃酸过多,故氢氧化钠也可以 |
4.小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁.铜的活动性强弱,遨请你一同参与.
【知识回放】金属活动性顺序:K Ca Na Mg Al ZnFe Sn Pb(H) Hg Ag Pt Au.请你在横线上填写对应金属的元素符号.
【做出猜想】猜想l:Cr>Fe>Cu;猜想2:Fe>Cu>Cr;猜想 3:你的猜想是Fe>Cr>Cu.
【査阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜
(2)铬能与稀硫酸反应.生成蓝色的硫酸亚铬(CrSO4)溶液
【设计与实验】小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
【结论与解择】
(1)小聪得到的结论是猜想1正确.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
【知识回放】金属活动性顺序:K Ca Na Mg Al ZnFe Sn Pb(H) Hg Ag Pt Au.请你在横线上填写对应金属的元素符号.
【做出猜想】猜想l:Cr>Fe>Cu;猜想2:Fe>Cu>Cr;猜想 3:你的猜想是Fe>Cr>Cu.
【査阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜
(2)铬能与稀硫酸反应.生成蓝色的硫酸亚铬(CrSO4)溶液
【设计与实验】小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 | 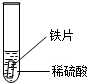 | 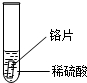 | 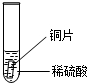 |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象发生 |
(1)小聪得到的结论是猜想1正确.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
1.图象和表格是数据表达的重要手段,根据下列图表回答问题.

表一 甲、乙分别在水、酒精中的溶解度
(1)分析表一数据可知,物质的溶解度受BCD(填序号)的影响.
A.溶剂质量 B.溶剂性质 C.溶质性质 D.温度
(2)比较表一、图1可知,图象与表格均能反映温度对固体物质溶解度的影响,其中图象的优点有AC(填序号).
A.数据更齐全 B.数据更精准 C.变化规律更直观
(3)若甲是NaOH,乙是Na2CO3,40℃时将CO2通入饱和的NaOH的酒精溶液,结合表一,写出该过程发生反应的化学方程式CO2+2NaOH═Na2CO3+H2O.
(4)40℃时,向两个盛有相同质量甲固体的烧杯中分别加入100g水和100g酒精,充分溶解后恢复至20℃,其结果如图2所示.下列说法中正确的是③(填序号).
①烧杯B中一定是不饱和溶液.
②烧杯B中的溶剂是酒精.
③升高温度或增加溶剂都有可能将A中固体全部溶解.
④若将烧杯A中溶液变为不饱和溶液,溶液中溶质质量分数一定减小.

表一 甲、乙分别在水、酒精中的溶解度
| 甲 | 乙 | |||
| 20℃ | 40℃ | 20℃ | 40℃ | |
| 水 | 109g | 129g | 21.8g | 49g |
| 酒精 | 17.3g | 40g | 不溶 | 不溶 |
A.溶剂质量 B.溶剂性质 C.溶质性质 D.温度
(2)比较表一、图1可知,图象与表格均能反映温度对固体物质溶解度的影响,其中图象的优点有AC(填序号).
A.数据更齐全 B.数据更精准 C.变化规律更直观
(3)若甲是NaOH,乙是Na2CO3,40℃时将CO2通入饱和的NaOH的酒精溶液,结合表一,写出该过程发生反应的化学方程式CO2+2NaOH═Na2CO3+H2O.
(4)40℃时,向两个盛有相同质量甲固体的烧杯中分别加入100g水和100g酒精,充分溶解后恢复至20℃,其结果如图2所示.下列说法中正确的是③(填序号).
①烧杯B中一定是不饱和溶液.
②烧杯B中的溶剂是酒精.
③升高温度或增加溶剂都有可能将A中固体全部溶解.
④若将烧杯A中溶液变为不饱和溶液,溶液中溶质质量分数一定减小.
8.正确操作是实验成功的保证.下列图示中,操作错误的是( )
| A. | 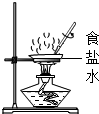 蒸发食盐水 | B. | 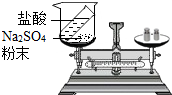 验证质量守恒定律 | ||
| C. | 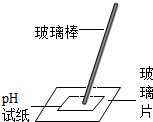 测定溶液的pH值 | D. | 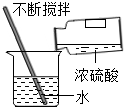 稀释浓硫酸 |
18.下列各组物质分别加入足量的水中,能共存且得到无色透明溶液的是( )
| A. | KNO3、HCl、NaNO3 | B. | K2CO3、Ba(NO3)2、NaCl | ||
| C. | KOH、HNO3、NaCl | D. | FeCl3、NaNO3、KCl |
5. 小明和小红在实验室发现了一瓶标签残缺的无色溶液(如图所示),为确认其中的溶质,他们设计并进行了如下探究活动,请回答下列问题.【观察与问题】这瓶试剂可能是什么溶液呢?
小明和小红在实验室发现了一瓶标签残缺的无色溶液(如图所示),为确认其中的溶质,他们设计并进行了如下探究活动,请回答下列问题.【观察与问题】这瓶试剂可能是什么溶液呢?
【交流与讨论】根据受损标签的情况判断,这瓶试剂不可能是A. A.酸 B.碱 C.盐
【猜想与假设】根据实际情况猜想溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种.
【资料查阅】上述四种物质的相关信息如下:
分析资料后,同学们排除了NaHCO3,他的判断依据是常温下碳酸氢钠饱和溶液的溶质质量分数为8.8%,到不到10%.
【实验与事实】
(1)小明用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>(填“>”、“<”或“=”)7,这瓶试剂不可能是NaCl.
(2)小红取该溶液少许于试管中,滴加氢氧化钙溶液,观察到有白色沉淀产生,由此确定溶质不是氢氧化钠,写出该操作中发生反应的化学方程式Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
【解释与结论】经过他们的努力,最终确定了该溶液中溶质的成分.
【拓展与反思】你认为在小红的实验中,除了选择氢氧化钙溶液外,还可以选择的药品是BC(填字母序号)
A.酚酞溶液 B.稀盐酸 C.氯化钡溶液.
 小明和小红在实验室发现了一瓶标签残缺的无色溶液(如图所示),为确认其中的溶质,他们设计并进行了如下探究活动,请回答下列问题.【观察与问题】这瓶试剂可能是什么溶液呢?
小明和小红在实验室发现了一瓶标签残缺的无色溶液(如图所示),为确认其中的溶质,他们设计并进行了如下探究活动,请回答下列问题.【观察与问题】这瓶试剂可能是什么溶液呢?【交流与讨论】根据受损标签的情况判断,这瓶试剂不可能是A. A.酸 B.碱 C.盐
【猜想与假设】根据实际情况猜想溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种.
【资料查阅】上述四种物质的相关信息如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
【实验与事实】
(1)小明用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>(填“>”、“<”或“=”)7,这瓶试剂不可能是NaCl.
(2)小红取该溶液少许于试管中,滴加氢氧化钙溶液,观察到有白色沉淀产生,由此确定溶质不是氢氧化钠,写出该操作中发生反应的化学方程式Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
【解释与结论】经过他们的努力,最终确定了该溶液中溶质的成分.
【拓展与反思】你认为在小红的实验中,除了选择氢氧化钙溶液外,还可以选择的药品是BC(填字母序号)
A.酚酞溶液 B.稀盐酸 C.氯化钡溶液.
2. 金属铯是一种金黄色,熔点低的活泼金属,是制造真空机器、光电管等的重要材料,铯的原子结构示意图及它在元素周期表中的某些信息如图所示,则下列说法正确的是( )
金属铯是一种金黄色,熔点低的活泼金属,是制造真空机器、光电管等的重要材料,铯的原子结构示意图及它在元素周期表中的某些信息如图所示,则下列说法正确的是( )
 金属铯是一种金黄色,熔点低的活泼金属,是制造真空机器、光电管等的重要材料,铯的原子结构示意图及它在元素周期表中的某些信息如图所示,则下列说法正确的是( )
金属铯是一种金黄色,熔点低的活泼金属,是制造真空机器、光电管等的重要材料,铯的原子结构示意图及它在元素周期表中的某些信息如图所示,则下列说法正确的是( )| A. | 铯的相对原子质量为55 | B. | 铯原子在反应中容易失去电子 | ||
| C. | 铯的原子序数为133 | D. | 铯原子的核外电子数为1 |
 如图牵手表示在一定条件下会发生化学反应.A、B、C、D、E分别是木炭、氧化铁、二氧化碳、稀盐酸、氢氧化钠中的一种物质,其中C是碱,E具有吸附性.
如图牵手表示在一定条件下会发生化学反应.A、B、C、D、E分别是木炭、氧化铁、二氧化碳、稀盐酸、氢氧化钠中的一种物质,其中C是碱,E具有吸附性.