题目内容
3.化学兴趣小组根据老师提供的实验装置(如图1)进行如下实验探究.(试剂足量,反应均完全,装置可重复使用,部分夹持装置已省略,装置气密性良好.)
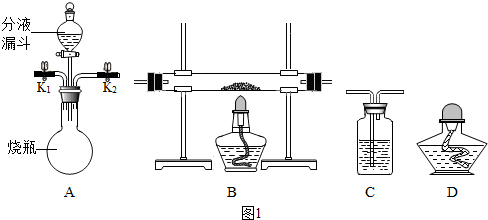
(1)甲组同学利用A装置中产生的氧气验证B中的黑色粉末是炭粉.
①A装置中反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②为完成此实验,除用A、B装置外,还需要补充C、D装置,C瓶中试剂为石灰水主要作用是证明有二氧化碳生成,反应化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O;
D装置的主要作用是提供热量.
(2)乙组同学要验证A中烧瓶内装的气体可能是CO、CO2、CH4中的一种或几种,为确定烧瓶内气体的成分,乙组同学进行如下实验(忽略B、C装置中空气的影响):
【资料】甲烷和氧化铜反应的化学方程式为:CH4+4CuO$\frac{\underline{\;\;△\;\;}}{\;}$4Cu+CO2+2H2O
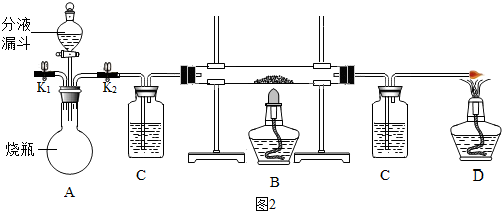
【操作步骤】
Ⅰ.按A→C→B→C→D的顺序连接装置如图2,实验时打开K2与分液漏斗,将3.0g的浓氢氧化钠溶液滴入烧瓶中;加热B中足量的氧化铜固体,点燃D中酒精灯.
Ⅱ.打开K1,通入氮气;待B中固体颜色不再发生改变,停止加热,继续通氮气.
Ⅲ.反应结束后,测得烧瓶中溶液的质量为3.1g,B中固体的质量减少了0.32g,
第二个C装置的质量增加了0.18g.
①在Ⅱ中打开K1,通入氮气目的是排出烧瓶中的气体;停止加热,继续通氮气目的是防止C中的液体倒吸入玻璃管中.
②两个C装置中试剂相同均为浓硫酸,则参加反应的氧化铜质量是1.6g.
③烧瓶中气体的成分为二氧化碳和甲烷.
分析 (1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
二氧化碳能和澄清石灰水中的氢氧化钙反应生成碳酸钙和水;
酒精灯是一种提供热量的仪器;
(2)氮气的化学性质不活泼;
浓硫酸能够吸收水;
根据提供的数据,通过计算可以确定气体的成分.
解答 解:(1)①A装置中,过氧化氢分解生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
②C瓶中试剂为石灰水主要作用是证明有二氧化碳生成,反应化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
D装置的主要作用是提供热量.
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;二氧化碳;Ca(OH)2+CO2═CaCO3↓+H2O;提供热量.
(2)①在Ⅱ中打开K1,通入氮气目的是排出烧瓶中的气体;
停止加热,继续通氮气目的是防止C中的液体倒吸入玻璃管中;
②设甲烷的质量为x,反应的氧化铜的质量为z,
第二个C装置的质量增加了0.18g,说明甲烷和氧化铜反应生成了0.18g水,
CH4+4CuO$\frac{\underline{\;\;△\;\;}}{\;}$4Cu+CO2+2H2O,
16 320 36
x z 0.18g
$\frac{16}{x}$=$\frac{320}{z}$=$\frac{36}{0.18g}$,
x=0.08g,z=1.6g,
设反应的氧化铜质量为y,
B中固体的质量减少了0.32g,说明反应的氧化铜中氧元素的质量是0.32g,根据题意有:$\frac{80}{16}$=$\frac{y}{0.32g}$,
y=1.6g,
因此混合气体中不含有一氧化碳;
反应结束后,测得烧瓶中溶液的质量为3.1g,说明气体中含有二氧化碳,质量为:3.1g-3.0g=0.1g,
即混合气体中含有二氧化碳和甲烷.
故填:排出烧瓶中的气体;防止C中的液体倒吸入玻璃管中;1.6;二氧化碳和甲烷.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
(2)20℃时,向一定量Ca(OH)2的饱和溶液中加入CaO,并保持温度不变,则所得溶液的质量减小(填“增大”、“减小”或“不变”,下同),溶液中溶质的质量分数不变.
| A. | 帕拉米韦中含有15个碳原子 | |
| B. | 帕拉米韦中碳元素的质量分数为54.9% | |
| C. | 帕拉米韦的相对分子质量为328g | |
| D. | 帕拉米韦分子中C、H、N、O的元素质量比为15:28:4:4 |
| A. | 真丝衬衣 | B. | 塑料水杯 | C. | 纯棉毛巾 | D. | 不锈钢锅 |
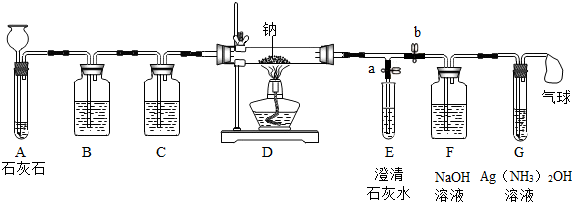
[提出猜想]CO2与Na反应可能产生4种物质:C、CO、Na2CO3和Na2O.
[查阅资料]①Na是非常活泼的金属,常温下能与O2、H2O等物质反应;②NaHCO3饱和溶液不与CO2反应;③Na2O是白色固体;④向银氨溶液[Ag(NH3)2OH]中通入CO产生灰色沉淀.
[实验过程]同学们在老师的指导下设计了如图所示装置(部分夹持仪器已略去).
(1)实验记录
| 序号 | 实验操作 | 主要实验现象 | 实验结论及解释 |
| ① | 打开a,关闭b,由长颈漏斗注入稀盐酸 | I.A中产生大量气泡 II.E中出现浑浊 | E中出现浑浊后,再点燃酒精灯的目的是:排出装置中的空气,防止空气的干扰 |
| ② | 当E中出现浑浊时,打开b,关闭a,点燃酒精灯 | I.D中Na剧烈燃烧,产生白烟.内壁附着黑色、白色固体 II.G中产生灰色沉淀 | D试管中的反应产物一定有C和CO |
| ③ | 取反应后D中少量白色固体于另一支试管中,加水溶解,再加入CaCl2稀溶液 | 产生白色沉淀 | D试管中的反应产物还有Na2CO3 |
①装置B可除去混杂在CO2中的HCl,写出该反应的化学方程式:NaHCO3+HCl=NaCl+CO2↑+H2O;
②若无装置C,对实验有影响的物质是水;
③写出E中出现浑浊所发生反应的化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O;
④[Ag(NH3)2OH]与CO反应,生成灰色沉淀Ag、碳酸铵和氨气,写出该反应的化学方程式:3Ag(NH3)2OH+CO=3Ag+(NH4)2CO3和4NH3↑.
| A. | 该研究有利于对环境无污染的清洁能源的开发 | |
| B. | 该研究有利于海水、污水的开发利用 | |
| C. | 该研究说明化学在材料、能源、环境和生命科学等方面发挥着重要的作用 | |
| D. | 该研究属于物理学及生物学范畴,没有涉及化学反应 |
