题目内容
下列现象说明了溶液的哪些性质:
①氢氧化钠溶液能使无色的酚酞试液变红,是因为它具有
②pH<5.6的雨水对大理石雕塑有较强的腐蚀性,是因为它具有
③电器着火时,不能用河水或自来水去灭火,是因为它具有
④煮沸的汤比开水要烫,是因为
⑤在北方冬天下雪的街道上要洒些氯化钠,其道理是
⑥浓硫酸和固体氢氧化钠都可以作某些气体的干燥剂,是因为它们都具有 .
①氢氧化钠溶液能使无色的酚酞试液变红,是因为它具有
②pH<5.6的雨水对大理石雕塑有较强的腐蚀性,是因为它具有
③电器着火时,不能用河水或自来水去灭火,是因为它具有
④煮沸的汤比开水要烫,是因为
⑤在北方冬天下雪的街道上要洒些氯化钠,其道理是
⑥浓硫酸和固体氢氧化钠都可以作某些气体的干燥剂,是因为它们都具有
考点:碱的化学性质,浓硫酸的性质及浓硫酸的稀释,酸雨的产生、危害及防治,氯化钠与粗盐提纯,灭火的原理和方法
专题:溶液、浊液与溶解度
分析:①根据碱性溶液能使酚酞变红色进行分析;
②根据溶液的酸碱性和pH值的关系进行分析;
③根据河水或自来水能够导电进行分析;
④根据水中溶解电解质后,能使使熔点升高进行分析;
⑤根据混合物的熔点比组成它的纯净物的熔点低进行分析;
⑥根据浓硫酸和氢氧化钠固体有吸水性进行分析.
②根据溶液的酸碱性和pH值的关系进行分析;
③根据河水或自来水能够导电进行分析;
④根据水中溶解电解质后,能使使熔点升高进行分析;
⑤根据混合物的熔点比组成它的纯净物的熔点低进行分析;
⑥根据浓硫酸和氢氧化钠固体有吸水性进行分析.
解答:解:①碱性溶液能使酚酞变红色,氢氧化钠溶液显碱性,所以氢氧化钠溶液能使无色的酚酞试液变红,是因为它具有碱性;
②pH<5.6的雨水对大理石雕塑有较强的腐蚀性,是雨水中的酸性物质和碳酸钙反应,所以是因为它具有酸性;
③河水或自来水能够导电,所以电器着火时,不能用河水或自来水去灭火,是因为它具有导电性;
④水中溶解电解质后,能使使熔点升高,所以煮沸的汤比开水要烫,是因为汤中溶解了一些电解质,所以沸点比纯水高;
⑤混合物的熔点比组成它的纯净物的熔点低,所以在北方冬天下雪的街道上要洒些氯化钠,其道理是溶液的凝固点降低
⑥浓硫酸和氢氧化钠固体有吸水性,所以浓硫酸和固体氢氧化钠都可以作某些气体的干燥剂,是因为它们都具有吸水性.
故答案为:①碱性;②酸性;③导电性;④汤中溶解了一些电解质,所以沸点比纯水高;⑤溶液的凝固点降低;⑥吸水性.
②pH<5.6的雨水对大理石雕塑有较强的腐蚀性,是雨水中的酸性物质和碳酸钙反应,所以是因为它具有酸性;
③河水或自来水能够导电,所以电器着火时,不能用河水或自来水去灭火,是因为它具有导电性;
④水中溶解电解质后,能使使熔点升高,所以煮沸的汤比开水要烫,是因为汤中溶解了一些电解质,所以沸点比纯水高;
⑤混合物的熔点比组成它的纯净物的熔点低,所以在北方冬天下雪的街道上要洒些氯化钠,其道理是溶液的凝固点降低
⑥浓硫酸和氢氧化钠固体有吸水性,所以浓硫酸和固体氢氧化钠都可以作某些气体的干燥剂,是因为它们都具有吸水性.
故答案为:①碱性;②酸性;③导电性;④汤中溶解了一些电解质,所以沸点比纯水高;⑤溶液的凝固点降低;⑥吸水性.
点评:本题主要考查了常见物的用途,要知道物质的性质是由物质的用途决定的,在平时的学习中要加强这方面的记忆.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图是电解水实验的装置图,有关该实验的叙述错误的是( )
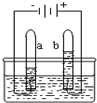

| A、该反应将电能转化为化学能 |
| B、试管b中的气体能使带火星的木条复燃 |
| C、产生的H2和O2的质量比为2:1 |
| D、该反应属于分解反应 |
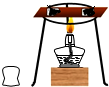 在如图实验中,铜片上左侧是滤纸片,右侧是乒乓球碎片.
在如图实验中,铜片上左侧是滤纸片,右侧是乒乓球碎片.