题目内容
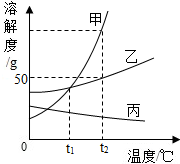 如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题:
如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题:(1)t2℃时,甲的溶解度
(2)t2℃时,向50克水中加入50g乙物质,充分溶解后所得溶液的质量是
(3)t1℃甲、乙、丙的饱和溶液升温到t2℃,所得溶液中溶质质量分数的大小关系为
(4)若固体乙中含有少量的甲,可用
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)据溶解度曲线可比较同一温度不同物质的溶解度大小;
(2)据该温度下乙的溶解度分析解答;
(3)据饱和溶液中溶质的质量分数计算方法和物质的溶解度受温度影响情况分析解答;
(4)据物质的溶解度受温度影响情况分析提纯乙的方法.
(2)据该温度下乙的溶解度分析解答;
(3)据饱和溶液中溶质的质量分数计算方法和物质的溶解度受温度影响情况分析解答;
(4)据物质的溶解度受温度影响情况分析提纯乙的方法.
解答:解:(1)t2℃时,甲的溶解度 大于乙的溶解度;
(2)t2℃时乙的溶解度是50g,即100g水中最多溶解50g的乙,所以向50克水中加入50g乙物质,充分溶解后最多溶解25g,所得溶液的质量是 75g;
(3)甲、乙的溶解度随温度升高而增大,乙的溶解度随温度升高而减小,所以t1℃甲、乙、丙的饱和溶液升温到t2℃,甲、乙的溶解度变大,变为不饱和溶液,溶质的质量分数与升温前相等,丙析出晶体,溶质的质量分数减小,据饱和溶液质量分数的计算式
×100%可知:溶解度大则溶质的质量分数大,而t1℃甲、乙溶解度相等且大于t2℃丙的溶解度,故所得溶液中溶质质量分数的大小关系为甲=乙>丙;
(4)由图可知:甲的溶解度受温度影响比乙大,所以若固体乙中含有少量的甲,可用蒸发结晶的方法提纯乙.
故答案为:(1)>;(2)75g;(3)甲=乙>丙;(4)蒸发结晶.
(2)t2℃时乙的溶解度是50g,即100g水中最多溶解50g的乙,所以向50克水中加入50g乙物质,充分溶解后最多溶解25g,所得溶液的质量是 75g;
(3)甲、乙的溶解度随温度升高而增大,乙的溶解度随温度升高而减小,所以t1℃甲、乙、丙的饱和溶液升温到t2℃,甲、乙的溶解度变大,变为不饱和溶液,溶质的质量分数与升温前相等,丙析出晶体,溶质的质量分数减小,据饱和溶液质量分数的计算式
| 溶解度 |
| 溶解度+100g |
(4)由图可知:甲的溶解度受温度影响比乙大,所以若固体乙中含有少量的甲,可用蒸发结晶的方法提纯乙.
故答案为:(1)>;(2)75g;(3)甲=乙>丙;(4)蒸发结晶.
点评:当一溶解度受温度变化影响大的物质中混入溶解度变化小的物质,要提纯溶解度变化影响大的用降温结晶的方法,反之,用蒸发结晶的方法提纯溶解度受温度变化影响小的物质.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
在下列各种情况下,埋在地下的铸铁输气管被腐蚀的速度最慢的是( )
| A、在呈酸性的潮湿土壤中 |
| B、在干燥 致密 不透气的土壤中 |
| C、在含沙粒较多 潮湿 透气的土壤中 |
| D、在潮湿 疏松透气的土壤中 |
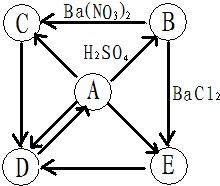 已知A是一种黑色单质,B、C、E是初中常见的盐,D是一种红色物质.下图是这物质的转化关系,部分反应物、生成物及反应条件已省略.
已知A是一种黑色单质,B、C、E是初中常见的盐,D是一种红色物质.下图是这物质的转化关系,部分反应物、生成物及反应条件已省略.
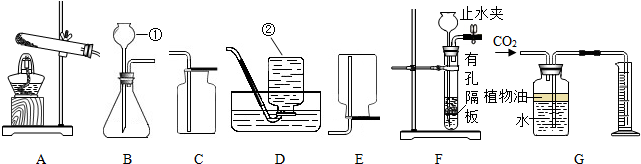
 “中心物质法”是化学复习过程中常用的一种学习方法,它是以一种物质为核心,通过发散思维,建立物质间的相互联系,从而把零碎的化学知识连成网络.已知A、B、C、D、E是初中化学常见的五种不同物质,A、E均是空气中常见的气体(说明:“--”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能向箭头所指方向转化,“←→”表示相连的两种物质能相互转化).试根据如图所示的关系回答下列问题:
“中心物质法”是化学复习过程中常用的一种学习方法,它是以一种物质为核心,通过发散思维,建立物质间的相互联系,从而把零碎的化学知识连成网络.已知A、B、C、D、E是初中化学常见的五种不同物质,A、E均是空气中常见的气体(说明:“--”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能向箭头所指方向转化,“←→”表示相连的两种物质能相互转化).试根据如图所示的关系回答下列问题: