题目内容
5.在56g10%的氢氧化钾溶液中加入一定量的硫酸,称得恰好完全反应后溶液的质量为80.5g.求:(1)加入的稀硫酸质量为24.5g;
(2)所用稀硫酸溶质的质量分数.
分析 根据质量守恒定律计算出稀硫酸的质量,根据氢氧化钾和稀硫酸恰好完全反应,由氢氧化钾的质量结合方程式可以计算出参加反应的硫酸溶质的质量,溶质的质量分数=$\frac{溶质的质量}{溶液的质量}$×100%分析解答.
解答 解:(1)稀硫酸溶液的质量=80.5 g-56 g=24.5 g 故答案为:24.5.
设所用稀硫酸溶质的质量为x
氢氧化钾质量=56 g×10%=5.6 g
H2SO4+2KOH═K2SO4+2H2O
98 112
x 5.6 g
$\frac{98}{x}=\frac{112}{5.6g}$
x=4.9g
所用稀硫酸溶质的质量分数=$\frac{4.9g}{24.5g}$×100%=20%
答:所用稀硫酸溶质的质量分数为20%.
点评 本题能较好考查学生应用质量守恒定律、溶质的质量分数等分析和解决问题的能力,解答时要注意格式规范.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列化学实验操作中正确的是( )
| A. | 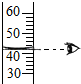 量取液体 | B. | 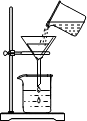 过滤 | C. | 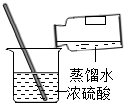 稀释浓硫酸 | D. | 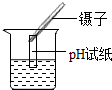 检测溶液pH |
20.如图是甲乙两位同学在学习碳酸钠的化学性质时所做的探究实验.
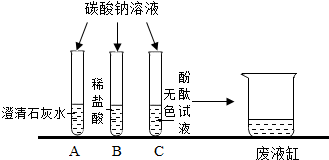
(1)A 中发生反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(2)B中发生化学反应的实质是氢离子与碳酸根离子反应生成水分子和二氧化碳分子.
(3)C中观察到的现象是酚酞试液变红色.
(4)将A、B、C三支试管内反应后的物质倒入废液缸中,发现废液澄清有气泡冒出,且酚酞溶液呈无色.
【提出问题】最终溶液中含有什么溶质?
【猜想与假设】
甲同学的猜想:废液中有氯化钙和氯化钠;
乙同学的猜想:废液中有氯化钙、氯化钠和氯化氢;
【活动与探究】为了验证甲、乙两位同学的猜想请你设计实验.
【交流反思】
最终废液的正确处理方法是加入适量熟石灰中和后排放.

(1)A 中发生反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(2)B中发生化学反应的实质是氢离子与碳酸根离子反应生成水分子和二氧化碳分子.
(3)C中观察到的现象是酚酞试液变红色.
(4)将A、B、C三支试管内反应后的物质倒入废液缸中,发现废液澄清有气泡冒出,且酚酞溶液呈无色.
【提出问题】最终溶液中含有什么溶质?
【猜想与假设】
甲同学的猜想:废液中有氯化钙和氯化钠;
乙同学的猜想:废液中有氯化钙、氯化钠和氯化氢;
【活动与探究】为了验证甲、乙两位同学的猜想请你设计实验.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量废液于试管中,向其中加入. | 有气泡冒出 | 乙同学猜想正确 |
最终废液的正确处理方法是加入适量熟石灰中和后排放.
10.下列分类和举例正确的是( )
| A. | 纯净物:碘盐、蒸馏水、二氧化碳气体 | |
| B. | 单质:干冰、晶体、氧气 | |
| C. | 导体:铁丝、稀盐酸、铜丝 | |
| D. | 绝缘体:陶瓷、石墨、橡胶 |

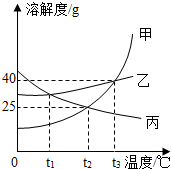 如图为甲、乙、丙三种固体物质的溶解度曲线,请回复.
如图为甲、乙、丙三种固体物质的溶解度曲线,请回复.