题目内容
18.如图是实验室制取CO2,并验证CO2和CO的性质的实验,请看图后回答问题.
(1)写出标有序号的仪器名称①长颈漏斗 ②铁架台.
(2)A中的反应方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
(3)B中的反应方程式为CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(4)C中的现象是黑色固体逐渐变为红色,固体逐渐减少,反应方程式为CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(5)D中的现象是澄清石灰水变浑浊,反应方程式为Ca(OH)2+CO2═CaCO3↓+H2O.
(6)E处的现象是气体燃烧,产生淡蓝色的火焰,反应方程式为2CO+O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2.
分析 题中图是实验室制取CO2,并验证CO2和CO的性质的实验:
(1)熟记常用仪器;
(2)用碳酸钙和盐酸制取二氧化碳;
(3)二氧化碳和碳高温下反应生成一氧化碳;
(4)一氧化碳还原黑色固体氧化铜,生成红色的铜;
(5)检验生成的气体是否为二氧化碳;
(6)点燃尾气,防止污染空气.
解答 解:(1)熟记常用仪器:①长颈漏斗;②铁架台;
(2)A中碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)B中一氧化碳与碳反应生成二氧化碳,化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
(4)C中一氧化碳高温下还原氧化铜:①现象:黑色固体逐渐变为红色,固体逐渐减少;②化学方程式为:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
(5)D中用澄清石灰水检验二氧化碳:①现象:澄清石灰水变浑浊;②化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
(6)E处点燃尾气:①现象:气体燃烧,产生淡蓝色的火焰;②化学方程式2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
故答案为:
(1)长颈漏斗;铁架台;
(2)CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
(4)黑色固体逐渐变为红色,固体逐渐减少;CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
(4)澄清石灰水变浑浊;Ca(OH)2+CO2═CaCO3↓+H2O;
(5)气体燃烧,产生淡蓝色的火焰;2CO+O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2.
点评 本题主要考查二氧化碳和一氧化碳的化学性质及应用,掌握二氧化碳和一氧化碳的化学性质和一些常用的化学方程式,学会分析反应现象和本质的联系.

 阅读快车系列答案
阅读快车系列答案| A. | 活性炭吸附有色气体 | B. | 氢气用做燃料 | ||
| C. | 液态氮做制冷剂 | D. | 用钨丝制作白炽灯丝 |
| A. | 铁管在潮湿的空气中不易锈蚀 | B. | 浓溶液一定是饱和溶液 | ||
| C. | 天然气泄漏,点火寻找泄漏处 | D. | 体温计中的水银属于金属材料 |
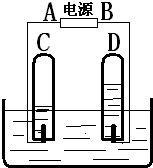 如图是电解水的简易装置.根据观察到的实验现象回答下列问题:
如图是电解水的简易装置.根据观察到的实验现象回答下列问题: .
.