题目内容
2.柠檬酸亚铁是重要的含铁试剂,兴趣小组制取柠檬酸亚铁溶液的实验流程如图: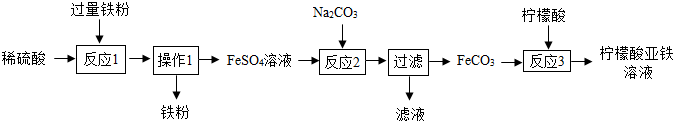
(1)写出反应1的化学方程式Fe+H2SO4=FeSO4+H2↑,该反应是否属于复分解反应否(填“是”或“否”);
(2)操作1的名称为过滤;
(3)写出反应2的化学方程式FeSO4+Na2CO3=FeCO3↓+Na2SO4;
(4)反应3中会有气体生成,该气体是二氧化碳;
(5)柠檬酸亚铁的化学式为FeC6H6O7,柠檬酸亚铁中铁元素和碳元素质量比为7:9,铁元素化合价为+2价.
分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:
(1)反应1是铁与硫酸反应,生成硫酸亚铁和氢气,对应的化学方程式为Fe+H2SO4=FeSO4+H2↑,是单质和化合物反应生成新的单质和新的化合物,而不是两种化合物相互交换成分生成两种新的化合物,所以不是复分解反应;
(2)操作1是实现难溶性固体铁和可溶性物质硫酸亚铁分离的过程,所以为过滤;
(3)反应2,反应物为硫酸亚铁和碳酸钠,而根据右侧可以看出生成难溶性的碳酸亚铁,根据复分解反应特点和质量守恒定律可知另一生成物为硫酸钠,也符合得到滤液的要求(硫酸钠易溶).所以对应的化学方程式为:FeSO4+Na2CO3=FeCO3↓+Na2SO4;
(4)反应3是碳酸亚铁和柠檬酸反应生成了柠檬酸亚铁,根据盐和酸反应生成新盐和新酸和质量守恒定律,可知过程生成不稳定的碳酸,碳酸不稳定,分解成二氧化碳和水,所以该气体为二氧化碳;
(5)柠檬酸亚铁的化学式为FeC6H6O7,由于名称中出现“亚铁”,所以所含铁元素的化合价为+2价,而柠檬酸亚铁中铁元素和碳元素质量比为56:(12×6)=7:9
故答案:
(1)Fe+H2SO4=FeSO4+H2↑,否;
(2)过滤;
(3)FeSO4+Na2CO3=FeCO3↓+Na2SO4;
(4)二氧化碳;
(5)7:9;+2价.
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.某钙片的标签如图,且知钙片成分中只有碳酸钙中含有钙元素:
(1)由标签信息可知,每片钙片(碳酸钙与其它辅助剂)质量为0.8克,请通过计算推断此标签中说每片钙片含钙元素质量0.75克是虚假的.
(2)某实验小组为测定其真实的含钙量做了如下实验,取10片钙片放入已称量的含足量盐酸的烧杯中,充分反应后再称取烧杯和剩余物质的总质量,数据如表:
①请列式计算每片此钙片含碳酸钙的质量.
②请列式计算每片此钙片的含钙元素质量.
(1)由标签信息可知,每片钙片(碳酸钙与其它辅助剂)质量为0.8克,请通过计算推断此标签中说每片钙片含钙元素质量0.75克是虚假的.

(2)某实验小组为测定其真实的含钙量做了如下实验,取10片钙片放入已称量的含足量盐酸的烧杯中,充分反应后再称取烧杯和剩余物质的总质量,数据如表:
| 物质的质量 | |
| 反应前:烧杯+盐酸 | 22g |
| 10片钙片 | 8g |
| 反应后:烧杯+剩余物 | 26.7g |
②请列式计算每片此钙片的含钙元素质量.
10.原子不显电性是因为( )
| A. | 原子不能得失电子 | B. | 原子中没有带电微粒 | ||
| C. | 原子中的中子数与质子数相等 | D. | 原子中核电荷数等于核外电子总数 |
7.下列对催化剂描述正确的是( )
| A. | 任何化学反应都需要催化剂 | |
| B. | 催化剂在反应前后本身的质量发生了变化 | |
| C. | 只有分解反应才需要催化剂 | |
| D. | 催化剂在反应前后化学性质不变 |
14.硫酸铜和氢氧化钠反应方程式为:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4,该反应属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
11.下列有关水的叙述正确的是( )
| A. | 大量使用农药、化肥不会污染水 | B. | 经常饮用蒸馏水对身体有益 | ||
| C. | 蔗糖水溶液能导电 | D. | 肥皂水鉴别硬水与软水 |
 2015年11月首架C919大飞机总装下线,标志着我国跻身飞机研制先进国家行列.
2015年11月首架C919大飞机总装下线,标志着我国跻身飞机研制先进国家行列.