题目内容
某兴趣小组为测定一包碳酸钠样品中碳酸钠的质量分数,进行实验.测得相关数据如图所示:
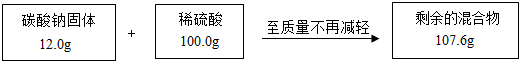
提示:①反应原理Na2CO3+H2SO4═NaSO4+H2O+CO2↑
②样品中的杂质不参加反应
③计算结果保留一位小数
(1)根据质量守恒定律,反应生成二氧化碳的质量为 g.
(2)计算该样品中碳酸钠的质量分数.(写出计算过程)

提示:①反应原理Na2CO3+H2SO4═NaSO4+H2O+CO2↑
②样品中的杂质不参加反应
③计算结果保留一位小数
(1)根据质量守恒定律,反应生成二氧化碳的质量为
(2)计算该样品中碳酸钠的质量分数.(写出计算过程)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据质量守恒定律可知,反应前后混合物减少的质量就是生成二氧化碳的质量进行解答;
(2)根据二氧化碳的质量利用化学反应方程式可以求出样品中碳酸钠的质量,进而求出该样品中碳酸钠的质量分数即可.
(2)根据二氧化碳的质量利用化学反应方程式可以求出样品中碳酸钠的质量,进而求出该样品中碳酸钠的质量分数即可.
解答:解:(1)根据质量守恒定律可知,反应前后混合物减少的质量就是生成二氧化碳的质量,所以反应生成二氧化碳的质量=12.0g+100.0g-107.6g=4.4g;故填:4.4;
(2)设样品中碳酸钠的质量为x.
Na2CO3+H2SO4═NaSO4+H2O+CO2↑
106 44
x 4.4g
=
x=10.6g
该样品中碳酸钠的质量分数=
×100%=88.3%
答:该样品中碳酸钠的质量分数为88.3%.
(2)设样品中碳酸钠的质量为x.
Na2CO3+H2SO4═NaSO4+H2O+CO2↑
106 44
x 4.4g
| 106 |
| x |
| 44 |
| 4.4g |
x=10.6g
该样品中碳酸钠的质量分数=
| 10.6g |
| 12g |
答:该样品中碳酸钠的质量分数为88.3%.
点评:本题考查了学生依据方程式计算的能力,同时考查了物质的纯度及溶液中溶质的质量分数.

练习册系列答案
相关题目
下列化学符号中,只具有微观意义的是( )
| A、H2 |
| B、Fe |
| C、3H |
| D、Fe2O3 |

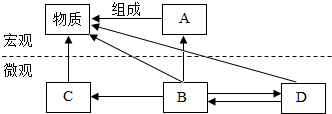 原子、分子、离子都是构成物质的微观离子,比如二氧化碳是由
原子、分子、离子都是构成物质的微观离子,比如二氧化碳是由