题目内容
20.下列叙述正确的是( )| A. | 可用盐酸除去铝粉中的锌粉 | B. | 铜在潮湿的空气中一般不会生锈 | ||
| C. | 锌、铁等金属能置换出酸中的氢气 | D. | 汞是金属,它在常温下呈液态 |
分析 铝能和稀盐酸反应生成氯化铝和氢气,锌能和稀盐酸反应生成氯化锌和氢气;
铜在在潮湿的空气中,能和水、氧气和二氧化碳反应生成碱式碳酸铜;
铁能和稀盐酸反应生成氯化亚铁和氢气;
汞是金属,它在常温下呈液态.
解答 解:A、铝能和稀盐酸反应生成氯化铝和氢气,锌能和稀盐酸反应生成氯化锌和氢气,因此不能用盐酸除去铝粉中的锌粉;
B、铜在在潮湿的空气中,能和水、氧气和二氧化碳反应生成碱式碳酸铜,因此铜在潮湿的空气中会生锈;
C、铁能和稀盐酸反应生成氯化亚铁和氢气,锌能和稀盐酸反应生成氯化锌和氢气,锌、铁等金属能置换出酸中的氢,而酸中不含有氢气,该选项说法不正确;
D、汞是金属,它在常温下呈液态,该选项说法正确.
故选:D.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
1.下列4个图象能正确反映对应变化关系是( )
| A. | 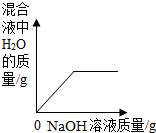 向一定量稀H2SO4中加入NaOH溶液 向一定量稀H2SO4中加入NaOH溶液 | |
| B. | 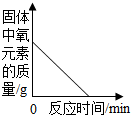 用酒精灯加热一定量KMnO4固体 用酒精灯加热一定量KMnO4固体 | |
| C. | 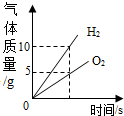 将水通电电解一段时间 将水通电电解一段时间 | |
| D. | 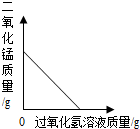 向一定量的二氧化锰中加入H2O2溶液 向一定量的二氧化锰中加入H2O2溶液 |
11.请根据如图所示的实验装置图填空.
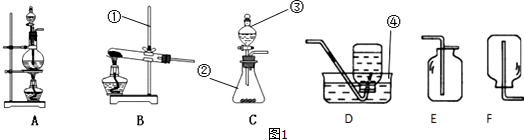
(1)指出图1中标有数字的仪器的名称:①铁架台,②锥形瓶,③分液漏斗,④水槽.
(2)在实验室用高锰酸钾制氧气时应该选择的发生装置是B,装置中还缺少一种实验用品棉花,其作用是防止固体进入导管.写出反应的文字(或符号)表达式:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气(或2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑).
(3)当用C装置制取氧气时,仪器③内盛放的液体是过氧化氢溶液,反应文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(4)在实验室制取并收集二氧化碳可选用CE 装置(填字母编号),写出实验室制取二氧化碳反应的文字表达式:碳酸钙+盐酸→氯化钙+水+二氧化碳.验证二氧化碳收集满的方法是燃着的木条放在集气瓶口.
(5)氢气是一种密度比空气小的气体,难溶于水.实验室常用金属锌粒和稀硫酸在常温下反应来制取氢气.实验室制取氢气的发生装置可以选择上图中的C装置,收集氢气可以选择上图中的D或F装置.
(6)实验室用加热二氧化锰和浓盐酸混合物的方法制取氯气,应该选择的发生装置是A.
(7)图2所示装置也可以用来收集气体.如果用该装置收集二氧化碳,气体应该从A导管通入.如果用排水法收集氧气,应该先在该装置中装满水,然后将氧气从B导管通入.
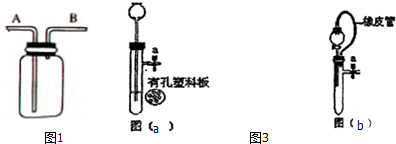
(8)小宋同学对气体发生装置作了改进,设计了如图3的装置,如图3(a)所示.使用图3(a)装置制取CO2,反应进行过程中,关闭该装置中的止水夹a后,可以观察到的现象液体被压回长颈漏斗中,固液分离,反应停止.
(9)小亮同学也改进了气体发生装置,改进的装置如图3(b)所示,与C装置相比较,橡皮管的作用是平衡气压或使分液漏斗和试管中的压强一致,便于液体滴落下来.
(10)小明同学探究了影响双氧水分解速度的某种因素.实验数据记录如下:
实验结论:在相同条件下,双氧水的浓度越大,双氧水分解得越快.

(1)指出图1中标有数字的仪器的名称:①铁架台,②锥形瓶,③分液漏斗,④水槽.
(2)在实验室用高锰酸钾制氧气时应该选择的发生装置是B,装置中还缺少一种实验用品棉花,其作用是防止固体进入导管.写出反应的文字(或符号)表达式:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气(或2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑).
(3)当用C装置制取氧气时,仪器③内盛放的液体是过氧化氢溶液,反应文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(4)在实验室制取并收集二氧化碳可选用CE 装置(填字母编号),写出实验室制取二氧化碳反应的文字表达式:碳酸钙+盐酸→氯化钙+水+二氧化碳.验证二氧化碳收集满的方法是燃着的木条放在集气瓶口.
(5)氢气是一种密度比空气小的气体,难溶于水.实验室常用金属锌粒和稀硫酸在常温下反应来制取氢气.实验室制取氢气的发生装置可以选择上图中的C装置,收集氢气可以选择上图中的D或F装置.
(6)实验室用加热二氧化锰和浓盐酸混合物的方法制取氯气,应该选择的发生装置是A.
(7)图2所示装置也可以用来收集气体.如果用该装置收集二氧化碳,气体应该从A导管通入.如果用排水法收集氧气,应该先在该装置中装满水,然后将氧气从B导管通入.

(8)小宋同学对气体发生装置作了改进,设计了如图3的装置,如图3(a)所示.使用图3(a)装置制取CO2,反应进行过程中,关闭该装置中的止水夹a后,可以观察到的现象液体被压回长颈漏斗中,固液分离,反应停止.
(9)小亮同学也改进了气体发生装置,改进的装置如图3(b)所示,与C装置相比较,橡皮管的作用是平衡气压或使分液漏斗和试管中的压强一致,便于液体滴落下来.
(10)小明同学探究了影响双氧水分解速度的某种因素.实验数据记录如下:
| 双氧水的质量 | 双氧水的浓度 | MmO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
5.山楂花是一种绿色保健食品,其主在成分是柠檬醛.现从山楂油中提取了7.6g柠檬醛,使其在氧气里完全燃烧,生成22g二氧化碳和7.2g水,则柠檬醛中( )
| A. | 只有碳、氢元素 | B. | 一定含有碳、氢、氧元素 | ||
| C. | 一定有碳、氢元素,可能有氧元素 | D. | 碳氢元素质量比30:4 |

 液化石油气是常用的燃料.请回答:
液化石油气是常用的燃料.请回答: 某化学兴趣小组对“制镁企业不能使用CO2作为消防器材”的问题进行探讨,请你参与他们的活动.
某化学兴趣小组对“制镁企业不能使用CO2作为消防器材”的问题进行探讨,请你参与他们的活动.