题目内容
用NaCl,CaCl2,AlCl3溶液分别与相同质量分数的AgNO3溶液反应,生成等质量氯化银沉淀,则它们所消耗的AgNO3溶液的质量比为( )
| A、1:1:1 | ||||
| B、3:2:1 | ||||
| C、1:2:3 | ||||
D、1:
|
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据反应的方程式Cl-+Ag+=AgCl↓结合物质的组成进行解答.
解答:解:根据反应的方程式Cl-+Ag+=AgCl↓,要想得到等质量的AgCl沉淀,则所消耗的AgNO3溶液中银离子的质量相同,所以所消耗的AgNO3溶液的质量相同,故用NaCl,CaCl2,AlCl3溶液分别与相同质量分数的AgNO3溶液反应,生成等质量氯化银沉淀,则它们所消耗的AgNO3溶液的质量比为1:1:1.
故选:A.
故选:A.
点评:本题考查了质量守恒定律及其应用、根据化学反应方程式的计算.解答该题时,利用了Cl的质量守恒定律.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
有一种不纯的K2CO3固体,可能含有Na2CO3、MgCO3、CuSO4、NaCl中的一种或几种.取该样品13.8g加入100g稀盐酸,恰好完全反应得到无色溶液,同时产生气体4.4g.下列判断正确的是( )
| A、完全反应得到无色溶液,样品中一定有CuSO4 |
| B、NaCl不与盐酸反应,样品中一定没有NaCl |
| C、Na2CO3和MgCO3都能和盐酸反应生成气体,样品中一定有Na2CO3和MgCO3 |
| D、所加稀盐酸中溶质的质量分数为7.3% |
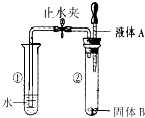 如图所示,打开止水夹,将液体A滴入试管②中与固体B接触.若试管①中的导管口没有气泡产生,则液体A和固体B的组合可能是下列中的( )
如图所示,打开止水夹,将液体A滴入试管②中与固体B接触.若试管①中的导管口没有气泡产生,则液体A和固体B的组合可能是下列中的( )| A、双氧水和MnO2 |
| B、水和生石灰 |
| C、稀盐酸和碳酸钠 |
| D、水和氯化钠 |
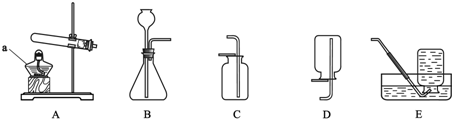
 小明同学欲测定石灰石样品中碳酸钙的质量分数(杂质不溶于水和酸且受热不分解),设计了下列实验方案:先称取8克石灰石样品,再把40克稀盐酸分4次加入,测量过程所得数据见下表:
小明同学欲测定石灰石样品中碳酸钙的质量分数(杂质不溶于水和酸且受热不分解),设计了下列实验方案:先称取8克石灰石样品,再把40克稀盐酸分4次加入,测量过程所得数据见下表: