题目内容
1.现欲探究一固体混合物A的成分,已知其中可能含有Mg(OH)2、CuO、NH4NO3、(NH4)2SO4四种物质中的一种或多种.如图所示进行实验,出现的现象如图所示(设过程中所有的化学反应均恰好完全反应).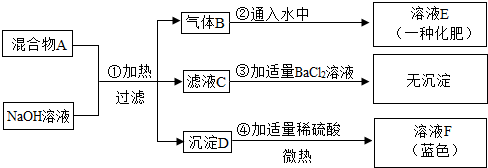
(1)溶液E的名称过滤.
(2)根据步骤③可知混合物A中,一定不存在的物质是(NH4)2SO4(写化学式).
(3)写出步骤①的化学方程式NH4NO3+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaNO3+H2O+NH3↑.
(4)如果溶液F只有一种溶质,则混合物A含有的物质化学式是CuO、NH4NO3,写出步骤④的化学方程式CuO+H2SO4=CuSO4+H2O.
分析 根据质量守恒定律即可推测,沉淀D和稀硫酸生成F(蓝色),说明F是硫酸铜,沉淀D是氧化铜,可能有氢氧化镁,说明混合物中含有氧化铜或者氢氧化镁;滤液C和氯化钡无明显现象,说明C中没有硫酸根,也说明混合物中没(NH4)2SO4.气体B和水生成E(化肥),说明B是氨气,E是氨水,也说明混合物中含有NH4NO3,可以据此来分析并完成解答.
解答 解:根据质量守恒定律即可推测,沉淀D和稀硫酸生成F(蓝色),说明F是硫酸铜,沉淀D是氧化铜,可能有氢氧化镁,说明混合物中含有氧化铜,可能有氢氧化镁;滤液C和氯化钡无明显现象,说明C中没有硫酸根,也说明混合物中没有(NH4)2SO4.气体B和水生成E(化肥),说明B是氨气,E是氨水,也说明混合物中含有NH4NO3,所以
(1)溶液E的名称过滤;
(2)根据步骤③可知混合物A中,一定不存在的物质是(NH4)2SO4;
(3)步骤①的反应是氢氧化钠和硝酸铵反应生成硝酸钠、水和氨气,化学方程式为:NH4NO3+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaNO3+H2O+NH3↑;
(4)如果溶液F只有一种溶质,则混合物A含有的物质化学式是CuO、NH4NO3,步骤④的反应是氧化铜和硫酸反应生成硫酸铜和水,化学方程式为:CuO+H2SO4═CuSO4+H2O.
故答案为:(1)过滤;
(2)(NH4)2SO4;
(3)NH4NO3+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaNO3+H2O+NH3↑;
(4)CuO、NH4NO3,CuO+H2SO4═CuSO4+H2O.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

 口算题天天练系列答案
口算题天天练系列答案| A. | HCl、KNO3、NaHCO3 | B. | MgSO4、AlCl3、NaNO3 | ||
| C. | NH4Cl、Na2SO4、KOH | D. | H2SO4、FeCl3、Ba(NO3)2 |
| A. | 可以用醋酸来检验烧碱是否变质 | |
| B. | 酸是指在通电条件下产生的阳离子全部是氢离子的化合物 | |
| C. | 熟石灰和烧碱常用来中和酸性土壤 | |
| D. | 天然雨水具有弱酸性,雨水的酸性越强,pH越大 |
| A. | 5.55g | B. | 11.1g | C. | 22.29g | D. | 33.3g |