题目内容
9.下列实验设计不能达到实验目的是( )| 选项 | A | B | C | D |
| 实 验 设 计 |  |  |  |  2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 |
| 实验目的 | 红磷燃烧测定空气中氧气的含量 | 探究蜡烛燃烧后有二氧化碳生成 | 验证氢气的密度比空气小 | 验证质量守恒定律 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据红磷燃烧生成固体,使瓶内压强改变分析;
B、根据二氧化碳能使澄清石灰水变浑浊分析;
C、根据肥皂泡上升分析;
D、根据氢氧化钠和硫酸铜反应的特点分析.
解答 解:A、红磷燃烧生成固体,消耗瓶内的氧气,所以瓶内产生压强差,冷却后打开止水夹,进入水的量即氧气的量,故A方法正确;
B、二氧化碳能使澄清石灰水变浑浊,把内壁涂有石灰水烧杯罩在蜡烛火焰上方,澄清石灰水变浑浊,能证明石蜡燃烧后有二氧化碳生成,故B方法正确;
C、充满氢气的肥皂泡上升,说明氢气的密度比空气小,故C方法正确;
D、氢氧化钠和硫酸铜二者在密闭容器中反应,没有气体成分的交换,可以验证质量守恒定律,即使在敞口容器中反应也能验证质量守恒定律,故D方法正确;
故选项为:无.
点评 本题主要考查化学实验方案的设计与评价,学会用实验探究物质的性质或变化规律的方法和技巧是最大的收获.

练习册系列答案
相关题目
20.在日常生活中人们食用的食盐中常要加碘盐,其中的碘是以KI03的形式存在,则碘元素的化合价为( )
| A. | +5 | B. | +1 | C. | +2 | D. | -1 |
17.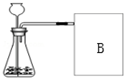 研究性学习小组选择“H2O2 溶液分解生成O2的反应快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
研究性学习小组选择“H2O2 溶液分解生成O2的反应快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】H2O2溶液分解生成O2的快慢与催化剂的种类有关.
【实验方案】常温下,在两瓶同质量、同浓度的H2O2 溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需要的时间.
B
【进行实验】右图是他们进行实验的装置图,反应的符号表达式为2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑;为了更容易准确地判断收集满氧气的时间,实验时B处宜采用的收集氧气方法是排水法.
【实验记录】(常温下,相同体积氧气.)
【结论】该探究过程得出的结论是:其它条件相同下,假设成立.
【反思】(1)H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快,若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的质量和化学性质是否改变.
(2)H2O2溶液分解生成O2的反应快慢还与哪些因素有关?反应物的质量分数(填一项即可)等,应控制好变量.
 研究性学习小组选择“H2O2 溶液分解生成O2的反应快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
研究性学习小组选择“H2O2 溶液分解生成O2的反应快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:【假设】H2O2溶液分解生成O2的快慢与催化剂的种类有关.
【实验方案】常温下,在两瓶同质量、同浓度的H2O2 溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需要的时间.
B
【进行实验】右图是他们进行实验的装置图,反应的符号表达式为2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑;为了更容易准确地判断收集满氧气的时间,实验时B处宜采用的收集氧气方法是排水法.
【实验记录】(常温下,相同体积氧气.)
| 实验编号 | 1 | 2 |
| 反应物 | 5%H2O2溶液 | 5%H2O2溶液 |
| 催化剂 | 1g水泥块 | 1gMnO2 |
| 时间 | 165秒 | 46秒 |
【反思】(1)H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快,若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的质量和化学性质是否改变.
(2)H2O2溶液分解生成O2的反应快慢还与哪些因素有关?反应物的质量分数(填一项即可)等,应控制好变量.
4.如图所示,下列各图所示的物质变化主要属于物理变化的是( )
| A. |  胆矾研碎 | B. |  蜡烛燃烧 | C. |  铁钉生锈 | D. |  火药爆炸 |
14. 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为因为镁燃烧是镁与空气中氧气等的反应.
(3)小红按图1装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
提出问题:黄色固体是什么呢?
查阅资料:①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
做出猜想:黄色固体是Mg3N2
实验探究:请设计实验,验证猜想
(4)为了证明镁可在氮气中燃烧生成氮化镁,小红又设计了如下方案进行验证.
步骤①:用盛水的水槽、无底的废广口瓶、燃烧匙、蒸发皿、橡皮塞等装配成如图2所示的装置;另准备一只有一根铜丝穿过的橡皮塞,铜丝末端固定一根镁条.
步骤②:引燃燃烧匙中足量的红磷,塞好橡皮塞;待充分冷却,观察
到广口瓶内水面上升的体积约占瓶内水面原上方空间的$\frac{1}{5}$左右.
步骤③:往水槽中加水使广口瓶内外水面相平;点燃镁条,迅速更换橡皮塞,镁条在广口瓶内继续燃烧,放出热量;待冷却后广口瓶内水位继续上升.
A.步骤②的目的是除尽空气中的氧气.写出红磷在氧气中燃烧的化学方程式4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5
B.在步骤③“待冷却后广口瓶内水位继续上升”是由于瓶内气压小于(选填“大于”“小于”或“等于”)外界气压
C.写出镁在氮气中燃烧生成氮化镁的化学方程式3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$ Mg3N2
反思与交流:
(5)空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO的质量却大于Mg3N2.请给出合理的解释O2比N2化学性质活泼.
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为因为镁燃烧是镁与空气中氧气等的反应.
(3)小红按图1装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
提出问题:黄色固体是什么呢?
查阅资料:①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
做出猜想:黄色固体是Mg3N2
实验探究:请设计实验,验证猜想
| 实验操作 | 实验现象及结论 |
| 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口 | 试管中有气体产生,湿润的红色石蕊试纸变蓝.证明猜想正确 |
步骤①:用盛水的水槽、无底的废广口瓶、燃烧匙、蒸发皿、橡皮塞等装配成如图2所示的装置;另准备一只有一根铜丝穿过的橡皮塞,铜丝末端固定一根镁条.
步骤②:引燃燃烧匙中足量的红磷,塞好橡皮塞;待充分冷却,观察
到广口瓶内水面上升的体积约占瓶内水面原上方空间的$\frac{1}{5}$左右.
步骤③:往水槽中加水使广口瓶内外水面相平;点燃镁条,迅速更换橡皮塞,镁条在广口瓶内继续燃烧,放出热量;待冷却后广口瓶内水位继续上升.
A.步骤②的目的是除尽空气中的氧气.写出红磷在氧气中燃烧的化学方程式4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5
B.在步骤③“待冷却后广口瓶内水位继续上升”是由于瓶内气压小于(选填“大于”“小于”或“等于”)外界气压
C.写出镁在氮气中燃烧生成氮化镁的化学方程式3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$ Mg3N2
反思与交流:
(5)空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO的质量却大于Mg3N2.请给出合理的解释O2比N2化学性质活泼.
1.水在化学实验中的应用很广泛.在做铁丝在氧气中燃烧的实验中,水的作用是( )
| A. | 溶解反应生成物 | B. | 作反应物 | C. | 作催化剂 | D. | 保护集气瓶 |
19.化学发展促进人类社会的发展,化学日益渗透到社会生产的各个方面.你认为下列各项不属于化学学科研究的范畴( )
| A. | 环境保护 | B. | 物质的组成、结构和性质 | ||
| C. | 认识自然、认识物质、应用物质 | D. | 研究地壳板块的运动规律 |
 A-F为初中化学中常见的物质,已知A为暗紫色固体,D为一种黑色粉末,它们的转化关系如图所示.请回答:
A-F为初中化学中常见的物质,已知A为暗紫色固体,D为一种黑色粉末,它们的转化关系如图所示.请回答: