题目内容
7.食盐是一种重要的化工原料.请回答下列问题.
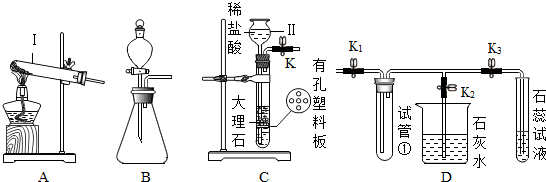
(1)请完善如图1实验室除去粗盐中泥沙等难溶性杂质的实验步骤.
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和漏斗.
②在蒸发过程中,待蒸发皿中出现较多固体时,停止加热,利用余热将滤液蒸干.
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制.流程如图2.
①加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是Na2CO3+BaCl2=BaCO3↓+2NaCl(用化学方程式表示)
②通过操作Ⅲ所得滤液中的溶质有NaOH、NaCl、Na2CO3(用化学式表示).
分析 (1)根据粗盐提纯的步骤和仪器以及注意事项进行分析;
(2)①根据碳酸钠可以除去反应中过量的氯化钡和氯化钙,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠进行分析;
②根据题中加入的各种除杂试剂进行分析.
解答 解:(1)去除泥沙的步骤是:①溶解:把粗盐放入烧杯中,加水溶解;②过滤:架好漏斗,使漏斗下端口紧贴烧杯内壁,沿玻璃棒把上述悬浊液慢慢导入漏斗中;该过程中用到的玻璃仪器主要有烧杯、玻璃棒和漏斗等;③蒸发结晶:将上述滤液倒入蒸发皿中,用酒精灯加热蒸发,待蒸发皿中出现较多量晶体时即停止加热;
(2)①碳酸钠可以除去反应中过量的氯化钡和氯化钙,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,化学方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl;
②通过分析可知,加入的碳酸钠、氢氧化钠都是过量的,还有生成的氯化钠,所以通过操作Ⅲ所得滤液中的溶质有NaOH、NaCl、Na2CO3.
故答案为:(1)①漏斗;
②蒸发皿中出现较多固体;
(2)①Na2CO3+BaCl2=BaCO3↓+2NaCl;
②NaOH、NaCl、Na2CO3.
点评 海水的综合利用是初中化学中较为重要的内容之一,与之相关的实验操作,药品的选用,化学方程式的书写等都是经常考查的内容,同学们一定要对此内容了然于心.

练习册系列答案
相关题目
17. 已知蜡烛的着火点约为190℃,蜡烛的火焰由气态蜡燃烧形成.如图所示,在温度计
已知蜡烛的着火点约为190℃,蜡烛的火焰由气态蜡燃烧形成.如图所示,在温度计
示数为280℃以上时,快速推动活塞,观察到蜡烛立即熄灭.蜡烛熄灭的主要原因是( )
 已知蜡烛的着火点约为190℃,蜡烛的火焰由气态蜡燃烧形成.如图所示,在温度计
已知蜡烛的着火点约为190℃,蜡烛的火焰由气态蜡燃烧形成.如图所示,在温度计示数为280℃以上时,快速推动活塞,观察到蜡烛立即熄灭.蜡烛熄灭的主要原因是( )
| A. | 隔绝氧气 | B. | 移走可燃物 | ||
| C. | 降低温度至着火点以下 | D. | 无法判断 |
18.生产、生活中的下列做法正确的是( )
| A. | 在室内放一盆水可以防止一氧化碳中毒 | |
| B. | 发现天然气泄漏,立即开启抽油烟机 | |
| C. | 用肥皂水区分硬水和软水 | |
| D. | 向刚刚用熟石灰改良过的酸性土壤中施用铵态氮肥 |
15.下列物质中,能和稀盐酸发生中和反应的是( )
| A. | Zn | B. | NaOH | C. | Fe2O3 | D. | CaCO3 |
12.下列实验操作正确的是( )
| A. |  取用固体 | B. |  滴加液体 | C. |  稀释浓硫酸 | D. |  熄灭酒精灯 |
16.常温下,下列各组物质中,甲既能与乙反应又能与丙反应的是( )
| 甲 | 乙 | 丙 | |
| A | Fe2O3 | CO | 稀盐酸 |
| B | H2 | Cl2 | CuO |
| C | Ba(NO3)2溶液 | 稀硫酸 | NaOH溶液 |
| D | CO2 | Ca(OH)2溶液 | H2O |
| A. | A | B. | B | C. | C | D. | D |