题目内容
17.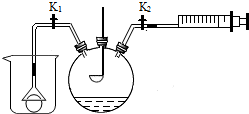 二氧化硫与二氧化碳具有某些相似的化学性质.为研究二氧化硫的性质,化学小组同学用如图所示装置进行实验.关闭K1、K2,将燃烧匙中硫粉在空气中点燃,迅速伸入如图所示瓶中,可以观察到火焰呈蓝紫色,则瓶内的气体是氧气,硫燃烧反应的化学方程式是S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.瓶内的石蕊溶液由紫色变为红色,原因是二氧化硫与水反应生成酸.
二氧化硫与二氧化碳具有某些相似的化学性质.为研究二氧化硫的性质,化学小组同学用如图所示装置进行实验.关闭K1、K2,将燃烧匙中硫粉在空气中点燃,迅速伸入如图所示瓶中,可以观察到火焰呈蓝紫色,则瓶内的气体是氧气,硫燃烧反应的化学方程式是S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.瓶内的石蕊溶液由紫色变为红色,原因是二氧化硫与水反应生成酸.(1)若只打开K1,烧杯内的乒乓球被吸在漏斗口,原因是二氧化硫溶于水,使瓶内气压减小.
(2)若注射器中盛有溶液A,只打开K2,可观察到的现象是注射器内的溶液A进入瓶中,瓶内溶液变为蓝色,溶液A一定具有的性质是显碱性.
(3)若注射器中盛有澄清石灰水,打开K1、K2,向外拉注射器,可观察到澄清石灰水变浑浊,反应的化学方程式是SO2+Ca(OH)2=CaSO3↓+H2O.
分析 本题能使同学们体会到实验探究的一般过程,通过实验分析可知:硫与氧气在点燃的条件下生成二氧化硫,二氧化硫与水反应生成亚硫酸,因此瓶内的石蕊溶液由紫色变为红色;只打开K1,烧杯内的兵乓球被吸在漏斗口,原因是二氧化硫溶于水,使瓶内气压减小,因此把小球吸起;若注射器中盛有溶液A,只打开K2,可观察到的现象是:注射器内的溶液A进入瓶中,因为内外产生了压强差;瓶内溶液变为蓝色,说明溶液A一定显碱性;打开K1、K2,向外拉注射器,可观察到澄清石灰水变浑浊,是因为二氧化硫与氢氧化钙反应生成亚硫酸钙白色沉淀和水,因此变浑浊.
解答 解:通过实验分析可知:硫与氧气在点燃的条件下生成二氧化硫,二氧化硫与水反应生成亚硫酸,因此瓶内的石蕊溶液由紫色变为红色;故答案为:氧气; S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;二氧化硫与水反应生成酸;
(1)只打开K1,烧杯内的兵乓球被吸在漏斗口,原因是二氧化硫溶于水,使瓶内气压减小,因此把小球吸起;故答案为:二氧化硫溶于水,使瓶内气压减小;
(2)若注射器中盛有溶液A,只打开K2,可观察到的现象是:注射器内的溶液A进入瓶中,因为内外产生了压强差;瓶内溶液变为蓝色,说明溶液A一定显碱性;故答案为:注射器内的溶液A进入瓶中;显碱性;
(3)打开K1、K2,向外拉注射器,可观察到澄清石灰水变浑浊,是因为二氧化硫与氢氧化钙反应生成亚硫酸钙白色沉淀和水,因此变浑浊;故答案为:SO2+Ca(OH)2=CaSO3↓+H2O.
点评 本考点既考查了实验步骤的设计和实验现象,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.本考点主要出现在实验题中.

 阅读快车系列答案
阅读快车系列答案| A. | 纯净物 | B. | 化合物 | C. | 非金属 | D. | 金属或合金 |
| A. | XY | B. | XY2 | C. | XY3 | D. | X2Y |
| A. | 分子可以构成物质,则物质一定是由分子构成的 | |
| B. | 离子是带电的原子或原子团,则带电的粒子都是离子 | |
| C. | 碱能使酚酞试液变红,则能使酚酞试液变红的物质一定是碱 | |
| D. | 单质是由同种元素组成的,则同种元素组成的纯净物一定是单质 |

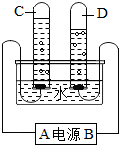 人类的日常生活和工农业生产都离不开水.请回答下列与水有关的问题:
人类的日常生活和工农业生产都离不开水.请回答下列与水有关的问题:
