题目内容
4.Ⅰ.用下列序号填空:①烧杯 ②试管 ③胶头滴管 ④燃烧匙能直接加热的玻璃仪器②;吸取或滴加少量液体的仪器③;
Ⅱ.通过一个月的化学学习,相信你已经初步掌握了实验室制取气体的有关知识.请结合图示回答问题:

(1)写出图中标示的仪器名称:①酒精灯,②集气瓶.
(2)实验室用高锰酸钾制取氧气,应选用的发生装置为D(填字母序号,下同),收集装置可选用F或G(写一种即可),取用高锰酸钾药品时,应选用仪器A,写出该反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)注射器C可用于检查装置E的气密性,步骤如下:
①向锥形瓶中加入少量水至浸没长颈漏斗下端处.
②将注射器C连接到装置E的导管口处.
③缓慢拉动注射器C的活塞,观察到长颈漏斗中水面下降,下端有气泡逸出,表示装置E的气密性良好.
④实验室用装置E制取氧气时,收集装置可选用F或G,检验氧气已收集满的方法是将带火星的木条放在集气瓶口,如果木条复燃,则证明已满.如用注射器C替换长颈漏斗,优点是可以控制反应的速率,写出制取该气体的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
分析 Ⅰ.首先考虑能直接加热的仪器有试管、蒸发皿、燃烧匙、坩埚,然后再选择玻璃仪器;胶头滴管用于少量液体的吸取;
Ⅱ.(1)熟悉常见仪器,了解名称;
(2)根据实验室用KMnO4制取O2,是固体的加热反应选择实验的发生装置;根据氧气的密度和溶水性选择收集装置;取用KMnO4药品时,要用药匙;
(3)用注射器C检查装置E的气密性时,向锥形瓶中加入少量水至浸没长颈漏斗下端,将注射器C连接到装置E的导管口处,缓慢拉动注射器C的活塞,观察现象.
(4)用装置E制取O2时,如用注射器C替换长颈漏斗,优点是可以控制反应的速率.
解答 解:Ⅰ.能直接加热的仪器有试管、蒸发皿、燃烧匙、坩埚,其中的玻璃仪器只有试管;少量液体的取用和滴加要用胶头滴管;
Ⅱ.:(1)图中①是酒精灯,②是集气瓶.
故答案为:①酒精灯;②集气瓶.
(2)实验室用KMnO4制取O2,是固体的加热反应,所以要选择装置D进行实验;氧气的密度大于空气的密度,并且不易溶于水,所以可以用排水法和向上排空气法收集;KMnO4是粉末状药品,要用药匙取用.
故答案为:D; F或G; A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)浸没长颈漏斗下端;长颈漏斗中水面下降,下端有气泡逸出.
(4)实验室用装置E制取氧气时,氧气不易溶于水,可以用排水法收集,密度比空气大,可以用向上排空气法收集;检验氧气已收集满的方法是将带火星的木条放在集气瓶口,如果木条复燃,则证明已满;注射器C替换长颈漏斗可以调节液体的流速,控制反应速度;用H2O2溶液和MnO2混合制氧气,其中MnO2起催化作用; 反应的方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
答案:Ⅰ.②;③;
Ⅱ.(1)①酒精灯;②集气瓶.
(2)D; F或G; A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)浸没长颈漏斗下端;长颈漏斗中水面下降,下端有气泡逸出;
(4)F或G;将带火星的木条放在集气瓶口,如果木条复燃,则证明已满;可以控制反应的速率;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
点评 解答本题关键是要知道常见仪器的名称和用途,知道发生装置和收集装置的选择方法,熟悉文字表达式的写法,知道二氧化碳不能用排水法收集,只能用向上排空气法收集,知道装置气密性的检查方法.

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案| A. | 限制使用塑料袋──节约资源 | B. | 石墨能导电──可作电极 | ||
| C. | 开采海底石油──开发新能源 | D. | 二氧化碳能与水反应──人工降雨 |
| A. | 氢气加氧气点燃生成水 | |
| B. | 每2个氢分子和1个氧分子在点燃条件下生成2个水分子 | |
| C. | 在点燃条件下,氢气和氧气反应生成水 | |
| D. | 在点燃条件下,每4份质量的氢气和32份质量的氧气反应生成36份质量的水 |
| A. | 食物变馊 | B. | 鞭炮爆炸 | C. | 冰雪融化 | D. | 铁生锈 |
| A. | 青蒿素是有15个碳原子、22个氢原子、5个氧原子构成的 | |
| B. | 青蒿素的相对分子质量为282g | |
| C. | 青蒿素中碳、氢元素质量比为15:22 | |
| D. | 青蒿素由碳、氢、氧三种元素组成 |
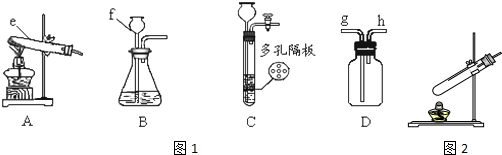
(1)图1中e、f仪器的名称:e试管,f长颈漏斗
(2)用氯酸钾和二氧化锰固体制氧气,选用的发生装置是A(填字母A、B、C、D),反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)用块状固体和液体不加热制取气体时,改用C装置(多孔隔板用来放块状固体)代替B装置的优点是随开随用、随关随停,容易控制.
(4)实验室里用双氧水和二氧化锰反应制氧气的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该实验不能(填“能”或“不能”)选用C装置,若用D装置来收集生成的氧气,气体应从g(填g或h)通入.
(5)同学们想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |
b.相同条件下,实验3(填实验编号)产生氧气的速率最快,说明双氧水的溶质质量分数越大反应速率越快.
(6)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水集气法收集气体,再检验,证明加热双氧水也可产生氧气.