题目内容
4.3月22日是“世界水日”,有关水的认识正确的是( )| A. | 生活中用活性炭降低水的硬度 | |
| B. | 将FeCl3、蔗糖、汽油分别接入一定量的水中都能形成溶液 | |
| C. | 自来水厂净水的过程有静置沉淀、过滤、吸附、消毒 | |
| D. | 从电解水得到H2和O2,可知水是由氢原子和氧原子组成的 |
分析 A、根据活性炭只能吸附色素和异味进行分析;
B、根据汽油难溶于水进行分析判断;
C、根据自来水厂净化水的方法进行分析判断.
D、根据水的组成分析.
解答 解:A、活性炭只能吸附色素和异味,不能降低水的硬度,故错误;
B、汽油难溶于水,加入一定量的水中,不会形成溶液,故错误;
C、自来水厂生产自来水时,使用的净水方法有沉淀、过滤、吸附、消毒,故正确;
D、电解水得到H2和O2,可知水是由氢元素和氧元素组成的,故错误.
故选C.
点评 加强有关水的知识的汇总和学习,有助于解答本类题.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
14.赣深高速是我国骨干干线-京九客运专线的一部分,它将于2016年开工建设.下列关于高铁建设过程中一定发生了化学变化的是( )
| A. | 石块粉碎 | B. | 扎实路基 | C. | 铁轨氧焊 | D. | 灯泡发光 |
15.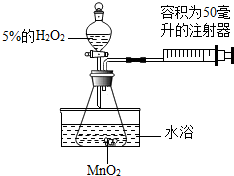 小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
(1)实验2中应加入5%H2O240毫升;
(2)在两次实验中,可通过相同的时间内注射器内气体的体积多少来比较H2O2分解反应速率的大小;
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有温度较高时水蒸发成水蒸气;
(4)实验结束后若要将MnO2从混合物汇总分离出来,可采取的方法是过滤、洗涤、干燥.
 小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:| 实验1 | 实验2 | |
| MnO2的质量/克 | 0.5 | 0.5 |
| 5%的H2O2的体积/毫升 | 40 | 待填 |
| 水浴温度/℃ | 20 | 80 |
(2)在两次实验中,可通过相同的时间内注射器内气体的体积多少来比较H2O2分解反应速率的大小;
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有温度较高时水蒸发成水蒸气;
(4)实验结束后若要将MnO2从混合物汇总分离出来,可采取的方法是过滤、洗涤、干燥.
12.下列各组离子在指定溶液中能大量共存的一组是( )
| A. | 在硝酸铵溶液中:Na+、Cu2+、OH- | B. | 在稀盐酸中:Ba2+、CO32-、Zn2+ | ||
| C. | 在氯化钠溶液中:K+、Ca2+、NO3- | D. | 在氢氧化钠溶液中:H+、Mg2+、Cl- |
19.化学兴趣小组探究金属的性质时,将一段去除氧化膜的镁条,放入一定量的稀盐酸中,有气泡产生,充分反应后静置,发现试管中有灰白色沉淀.
【提出问题】
灰白色沉淀是什么物质?
【猜想假设】
小华认为灰白色沉淀为碳酸镁(MgCO3),其他同学认为不需要实验就能否定小华的猜想,理由是反应物中没有碳元素,不会生成碳酸镁.
小宇认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体.
小彤认为灰白色沉淀为脱落的镁粉细颗粒.
【实验探究1】
基于以上探究与分析,原有猜想均遭到了否定.
【查阅资料】
HCl+AgNO3═HNO3+AgCl↓,AgCl是一种白色沉淀.
【实验探究2】
他们又另取灰白色沉淀放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了氯化氢气体.再将湿润的蓝色石蕊试纸悬于试管口,试纸变红色.
同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀.据文献介绍,碱式氯化镁存在多种组成结构,化学通式可表示为Mgx(OH)yClz•mH2O(其中2x-y-z=0,0≤m≤6).
【反思拓展】
(1)做镁与稀盐酸反应的实验时,镁条的用量宜少不宜多.
(2)铁片和铜片放入稀硫酸中产生的现象也不相同,据此推测出铁的活性比铜强.还可根据铁和硫酸铜溶液的反应来确定这两种金属的活动性强弱,该反应的化学方程式为Fe+CuSO4=FeSO4+Cu.
【提出问题】
灰白色沉淀是什么物质?
【猜想假设】
小华认为灰白色沉淀为碳酸镁(MgCO3),其他同学认为不需要实验就能否定小华的猜想,理由是反应物中没有碳元素,不会生成碳酸镁.
小宇认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体.
小彤认为灰白色沉淀为脱落的镁粉细颗粒.
【实验探究1】
| 实验操作 | 现象 | 结论 |
| ①取试管中的上层清液,加入适量的氯化镁固体 | 氯化镁固体 溶解(选填“溶解”或“不溶解”) | 小宇猜想错误 |
| ②取适量白色沉淀加入足量稀盐酸中 | 没有(选填“有”或“没有”)气泡冒出 | 小彤猜想错误 |
【查阅资料】
HCl+AgNO3═HNO3+AgCl↓,AgCl是一种白色沉淀.
【实验探究2】
他们又另取灰白色沉淀放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了氯化氢气体.再将湿润的蓝色石蕊试纸悬于试管口,试纸变红色.
同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀.据文献介绍,碱式氯化镁存在多种组成结构,化学通式可表示为Mgx(OH)yClz•mH2O(其中2x-y-z=0,0≤m≤6).
【反思拓展】
(1)做镁与稀盐酸反应的实验时,镁条的用量宜少不宜多.
(2)铁片和铜片放入稀硫酸中产生的现象也不相同,据此推测出铁的活性比铜强.还可根据铁和硫酸铜溶液的反应来确定这两种金属的活动性强弱,该反应的化学方程式为Fe+CuSO4=FeSO4+Cu.
16.下列成语中,涉及有化学变化的是( )
| A. | 滴水成冰 | B. | 火烧连营 | C. | 大海捞针 | D. | 刻舟求剑 |
13.下列物质属于纯净物的是( )
| A. | 汽水 | B. | 液态氧 | C. | 水泥砂浆 | D. | 洁净的空气 |