题目内容
9.中国高铁制造处于世界先进水平.2014年12月,乌鲁木齐-兰州高铁正式通车.(1)古丽同学乘高铁外出学习,她准备了在高铁上吃的食物有:油饼、风干肉、矿泉水.从营养合理搭配的角度考虑,还缺少的营养素有维生素,你认为还应补充苹果(填食物名称).
(2)高铁建设需要大量的材料,其中主要用到的有:A.金属材料、B.无机非金属材料、C.合成材料、D.复合材料.用对应字母填空.
①钒钢用于制造高铁的铁轨,它属于A.
②高铁座椅上常用到耐磨、耐腐蚀的涤纶等,涤纶属于C.
(3)高铁列车装有烟雾感应器,高速运行时是全封闭的.列车运行过程中在车厢内吸烟的危害是损害他人健康,而且车上的烟雾报警器就会发出警报,导致列车减速甚至自动停车.
分析 (1)根据人体所需六大营养素的种类、食物来源和合理膳食的原则,结合题中所给的食谱判断所含的营养素以及缺少的营养素,进行分析解答;
(2)根据材料的分类进行分析;
(3)根据列车运行过程中在车厢内吸烟的危害进行分析.
解答 解:(1)人体需要的六大营养物质:蛋白质、糖类、油脂、维生素、无机盐和水;结合题意,油饼中富含淀粉和油脂,淀粉属于糖类;风干肉中富含蛋白质,矿泉水中富含水,可知食物中维生素含量较少;故为使营养搭配更加合理,需要补充富含维生素的食物,如蔬菜、水果等;故填:维生素;苹果;
(2)①钒钢用于制造高铁的铁轨,它属于金属材料;故填:A.
②涤纶是合成纤维,属于有机合成材料;故填:C;
(3)新一代动车高铁列车属于全封闭式车厢,高铁运行过程中,一旦有人吸烟,车厢内就会烟雾弥漫,不仅损害他人健康,而且车上的烟雾报警器就会发出警报,导致列车减速甚至自动停车;故填:损害他人健康,而且车上的烟雾报警器就会发出警报,导致列车减速甚至自动停车.
点评 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.

练习册系列答案
相关题目
19.下列实验方案不合理的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 鉴别稀硫酸与氢氧化钠溶液 | 测定溶液的pH |
| B | 验证敞口放置的氢氧化钠溶液已变质 | 加盐酸 |
| C | 除去生石灰中少量的碳酸钙 | 向固体中加稀盐酸 |
| D | 除去氯化钠中少量的泥沙 | 加水溶解、过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
4.3月22日是“世界水日”,有关水的认识正确的是( )
| A. | 生活中用活性炭降低水的硬度 | |
| B. | 将FeCl3、蔗糖、汽油分别接入一定量的水中都能形成溶液 | |
| C. | 自来水厂净水的过程有静置沉淀、过滤、吸附、消毒 | |
| D. | 从电解水得到H2和O2,可知水是由氢原子和氧原子组成的 |
14. 要探究碳酸亚铁和氧气充分反应后的固体成分,请你参与华雪同学的探究:
要探究碳酸亚铁和氧气充分反应后的固体成分,请你参与华雪同学的探究:
【查阅资料】①碳酸亚铁(FeCO3)具有还原性,在空气中灼烧生成的氧化物和CO2气体.
②FeO是一种黑色粉末,它不稳定,在空气中加热,就迅速被氧化成四氧化三铁,四氧化三铁能与盐酸反应生成氯化亚铁、氯化铁和水.
③FeCl2能使高锰酸钾溶液褪色,而FeCl3不能;FeCl3溶液中滴加KSCN溶液,溶液变红色,FeCl2溶液中滴加KSCN溶液,溶液不出现红色.
【猜想与假设】猜想1:固体成分是氧化铁;
猜想2:固体成分是四氧化三铁;
猜想3:固体成分是氧化铁和四氧化三铁.
【活动与探究】连接仪器、装好药品如图所示(加热和固定装置已省略),打开止水夹K,通入氧气,加热玻璃管X.当Y瓶中产生的沉淀不再增加时,停止加热,继续通入氧气至玻璃管冷却.
取玻璃管里的少量固体于试管中,滴加盐酸,微热,固体完全溶解.将所得溶液分成甲、乙两份进行实验.
【结论与反思】(1)由上述实验现象可知,FeCO3在氧气中高温灼烧得到的固体产物是氧化铁,因此,猜想1(填“1”或“2”或“3”)是正确的.
(2)FeCO3在氧气中高温灼烧的化学方程式为4FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4CO2.
(3)上述实验a(填“a”或“b”)是多余的,因为无论是哪种猜想中的固体,溶于盐酸后溶液中都存在Fe3+,加入KSCN溶液后都会变红色,因此实验a不能判断固体的成分.
【总结与提升】(1)若实验结束时观察到Y瓶中仍然是澄清的,可能的原因是澄清石灰水的量不足,导致生成的碳酸钙转变成了可溶于水的碳酸氢钙.碳酸氢钙的化学式为Ca(HCO3)2.
(2)CO2使澄清石灰水变浑浊的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
(3)华雪同学经过反思,觉得该实验设计还存在问题,因为如果在实验b中观察到高锰酸钾溶液褪色,就不能确定哪个猜想是正确的.所以华雪同学又对该实验进行了定量探究:取11.6g纯净的碳酸亚铁固体,在空气中高温灼烧至恒重,称得固体质量净减3.6g.通过计算即可确定:FeCO3和氧气充分反应后的固体成分是氧化铁.
 要探究碳酸亚铁和氧气充分反应后的固体成分,请你参与华雪同学的探究:
要探究碳酸亚铁和氧气充分反应后的固体成分,请你参与华雪同学的探究:【查阅资料】①碳酸亚铁(FeCO3)具有还原性,在空气中灼烧生成的氧化物和CO2气体.
②FeO是一种黑色粉末,它不稳定,在空气中加热,就迅速被氧化成四氧化三铁,四氧化三铁能与盐酸反应生成氯化亚铁、氯化铁和水.
③FeCl2能使高锰酸钾溶液褪色,而FeCl3不能;FeCl3溶液中滴加KSCN溶液,溶液变红色,FeCl2溶液中滴加KSCN溶液,溶液不出现红色.
【猜想与假设】猜想1:固体成分是氧化铁;
猜想2:固体成分是四氧化三铁;
猜想3:固体成分是氧化铁和四氧化三铁.
【活动与探究】连接仪器、装好药品如图所示(加热和固定装置已省略),打开止水夹K,通入氧气,加热玻璃管X.当Y瓶中产生的沉淀不再增加时,停止加热,继续通入氧气至玻璃管冷却.
取玻璃管里的少量固体于试管中,滴加盐酸,微热,固体完全溶解.将所得溶液分成甲、乙两份进行实验.
| 实验编号 | 实验步骤 | 实验现象 |
| a | 向甲溶液中滴加KSCN溶液 | 溶液变红色 |
| b | 向乙溶液中滴加高锰酸钾溶液 | 高锰酸钾溶液的紫红色不消失 |
(2)FeCO3在氧气中高温灼烧的化学方程式为4FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4CO2.
(3)上述实验a(填“a”或“b”)是多余的,因为无论是哪种猜想中的固体,溶于盐酸后溶液中都存在Fe3+,加入KSCN溶液后都会变红色,因此实验a不能判断固体的成分.
【总结与提升】(1)若实验结束时观察到Y瓶中仍然是澄清的,可能的原因是澄清石灰水的量不足,导致生成的碳酸钙转变成了可溶于水的碳酸氢钙.碳酸氢钙的化学式为Ca(HCO3)2.
(2)CO2使澄清石灰水变浑浊的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
(3)华雪同学经过反思,觉得该实验设计还存在问题,因为如果在实验b中观察到高锰酸钾溶液褪色,就不能确定哪个猜想是正确的.所以华雪同学又对该实验进行了定量探究:取11.6g纯净的碳酸亚铁固体,在空气中高温灼烧至恒重,称得固体质量净减3.6g.通过计算即可确定:FeCO3和氧气充分反应后的固体成分是氧化铁.
1.下列做法符合环境保护要求的是( )
| A. | 回收废旧金属 | B. | 大量使用一次性塑料制品 | ||
| C. | 随意排放工业废水和生活污水 | D. | 实验室废物不经处理随意丢弃 |
18.下列实验操作中,正确的是( )
| A. | 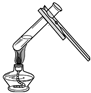 加热液体 | B. | 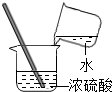 稀释浓硫酸 | C. | 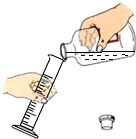 量取液体 | D. | 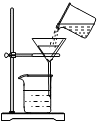 过滤 |