题目内容
【题目】“微观-宏观-符号”三重表征是化学独特的表示物质及其变化的思维方法。
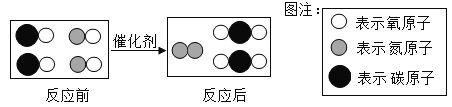
(1)下列是汽车尾气治理过程中有关化学反应的微观示意图。图中所示反应的化学方程式为___________________。
(2)某化学兴趣小组的同学探究了某些酸、碱、盐之间是否发生复分解反应。
内容 | 现象 | 实验解析 | 结论 | |
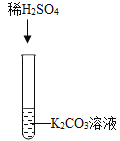
实验一 |
| ________ | 该反应的微观实质(用离子符号表示) :
| 复分解反应的实质是溶液中离子之间相互反应,生成__________ |
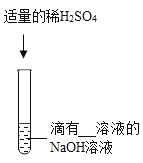
实验二 |
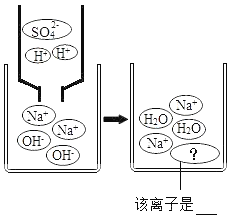
| 溶液颜色由红色恰好变为无色 |
| |
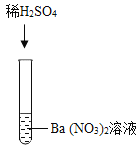
实验三 |
| 产生白色沉淀 | 该反应的微观实质(用离子符号表示) : ________ |
[迁移应用]下列离子在水中能大量共存,并形成无色溶液的是_______________(填字母)
a. Fe2+Na+NO3-Cl-
b. K+Na+OH- SO42-
c.H+K+SO42-OH-
d. Ba2+NO3-CO32-Cl-
【答案】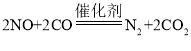 有气泡产生 CO32- 水、沉淀或气体 无色酚酞试液 SO42-
有气泡产生 CO32- 水、沉淀或气体 无色酚酞试液 SO42-
Ba2+ B
【解析】
(1)由微观示意图可知,该反应是由一氧化氮与一氧化碳在催化剂的作用下反应生成氮气和二氧化碳:![]() ;
;
(2)实验一:反应方程式是:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,观察到有气泡产生,该化学反应的实质是硫酸中的氢离子与碳酸钾中的碳酸根离子结合成水和二氧化碳,即2H++CO32-═H2O+CO2↑;
实验二:氢氧化钠溶液能使无色的酚酞试液变红色,加入适量的稀硫酸时,硫酸中的氢离子与氢氧化钠溶液中的氢氧根离子结合成水,恰好中和时,溶液呈中性,溶液由红色变成无色,反应方程式是:H2SO4+2NaOH=Na2SO4+2H2O,图示中的离子是硫酸根离子:SO42-;
实验三:硫酸与硝酸钡反应方程式是H2SO4+Ba(NO3)2=BaSO4↓+2HNO3,该反应的实质是硫酸中的硫酸根离子与硝酸钡中的钡离子结合成硫酸钡白色沉淀,即Ba2++SO42-═BaSO4↓;
由以上三个复分解反应可知,复分解反应的实质是溶液中离子之间相互反应,生成气体、水或沉淀;
[迁移应用]
a.含有Fe2+的溶液是浅绿色的,不符合题意;
b.四种离子间不能结合成沉淀、气体或水,能大量共存,且溶液是无色的,符合题意;
c.H+与OH-能结合成水,不能大量共存,不符合题意;
d.Ba2+与CO32-能结合成碳酸钙沉淀,不能大量共存,不符合题意。故选B。

 阅读快车系列答案
阅读快车系列答案