题目内容
实验室用过氧化氢溶液(过氧化氢与水的混合物)与二氧化锰混合制取氧气.现将50g过氧化氢溶液和1g二氧化锰混合物放入锥形瓶中,完全反应结束后,称得锥形瓶中剩余物质的质量为47.8g.计算:
(1)完全反应后产生氧气的质量为 g.
(2)过氧化氢溶液中过氧化氢的质量分数.
(1)完全反应后产生氧气的质量为
(2)过氧化氢溶液中过氧化氢的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据过氧化氢溶液和二氧化锰混合生成水和氧气,所以反应前后质量减少的就是氧气的质量进行解答;
(2)根据生成氧气的质量可以计算过氧化氢溶液中过氧化氢的质量,进而求出过氧化氢溶液中过氧化氢的质量分数即可.
(2)根据生成氧气的质量可以计算过氧化氢溶液中过氧化氢的质量,进而求出过氧化氢溶液中过氧化氢的质量分数即可.
解答:解:(1)过氧化氢溶液和二氧化锰混合生成水和氧气,所以反应前后质量减少的就是氧气的质量,所以氧气的质量=50g+1g-47.8g=3.2g;故填:3.2;
(2)设过氧化氢溶液中过氧化氢的质量分数为x
2H2O2
2H2O+O2↑
68 32
50g×x 3.2g
=
x═13.6%
答:过氧化氢溶液中过氧化氢的质量分数为13.6%.
(2)设过氧化氢溶液中过氧化氢的质量分数为x
2H2O2
| ||
68 32
50g×x 3.2g
| 68 |
| 50g×x |
| 32 |
| 3.2g |
x═13.6%
答:过氧化氢溶液中过氧化氢的质量分数为13.6%.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,差量法是正确快速解答此类题的捷径.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
将两种溶液混合未发生化学反应,所得溶液的pH等于3,则原来两种溶液的pH可能分别是( )
| A、2和10 | B、2和3 |
| C、2和7 | D、7和10 |
在一种由氮、氧两种元素组成的化合物中,测得其中氮、氧两种元素的质量比是7:4,该化合物是( )
| A、NO2 |
| B、N2O |
| C、N2O5 |
| D、NO |
下列事实不能证明空气中含水蒸气的是( )
| A、夏天清晨,草上有很多露珠 |
| B、对着干而冷的玻璃吹气,玻璃上出现一层水雾 |
| C、寒冷的冬天,窗户的玻璃上出现一层冰花 |
| D、饼干长时间露置于空气中会变得不酥脆 |
某一杯食盐水,若上部的密度为1.1g/cm3,则下部的密度是( )
| A、大于1.1g/cm3 |
| B、等于1.1g/cm3 |
| C、小于1.1g/cm3 |
| D、无法判断 |
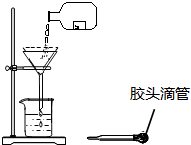 某同学进行如图所示的过滤操作,请完成下列空白:
某同学进行如图所示的过滤操作,请完成下列空白: