题目内容
12.中国科学家屠呦呦获2015年诺贝尔生理学或医学奖,她的团队从中药中分离出青蒿素应用于疟疾治疗,已知青蒿素的分子式为C15H22O5,下列说法正确的是( )| A. | 青蒿素属于氧化物 | |
| B. | 青蒿素中碳、氢、氧元素质量比为15:22:5 | |
| C. | 青蒿素由C、H、O 三种元素组成 | |
| D. | 青蒿素是由15 个碳原子、22 个氢原子和5 个氧原子构成 |
分析 A.根据氧化物的概念来分析;
B.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析;
C.根据青蒿素化学式的含义进行分析解答;
D.根据物质的结构来分析.
解答 解:A.氧化物中只能含有两种元素,而青蒿素是由三种元素组成的,故不属于氧化物,故错误;
B.青蒿素中碳、氢、氧三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40,故错误;
C.青蒿素是由碳、氢、氧三种元素组成的,故正确;
D.青蒿素是由青蒿素分子构成的,而不是由原子直接构成的,故错误.
故选C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
2.下列化学变化中吸收热量的是( )
| A. | 氢气还原氧化铜 | B. | 铁在氧气中燃烧 | C. | 锌和稀硫酸反应 | D. | 动植物的呼吸 |
20.下列反应属于氧化反应的是( )
| A. | HCl+NaOH═NaCl+H2O | B. | CaO+H2O═Ca(OH)2 | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 |
17.下列属于化学变化的是( )
| A. | 水沸腾变成水蒸气 | B. | 胆矾研碎 | ||
| C. | 铁锅生锈 | D. | 石蜡熔化 |
3.小丽同学在一次课外实验探究酸的化学性质时误将过氧化氢(H2O2)溶液当作酸与氧化铁(Fe2O3)粉末混合,发现有大量气泡产生.她联想到二氧化锰(MnO2)可作为H2O2分解的催化剂,那么,Fe2O3能否作为H2O2分解的催化剂呢?请你一起参与探究,并填写下列空白.
【猜想】Fe2O3能否作为H2O2分解的催化剂.
【实验验证】小丽同学一次设计了三个实验
实验一 取一定量的H2O2溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,观察到木条没有复燃,说明H2O2溶液常温下分解缓慢.
实验二 在实验一的试管中加入wg Fe2O3粉末,有大量气泡产生,然后伸入带火星的木条,观察到木条复燃,说明Fe2O3能加快H2O2的分解速率.
实验三 待反应结束后,将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为wg,说明反应前后Fe2O3的质量保持不变.
【实验结论】小丽同学认为,Fe2O3粉末可以作为H2O2分解的催化剂.
【反思评价】小江同学认为要证明小丽同学的结论正确,仅做这三个实验还不充分,需要补充一个探究实验,探究Fe2O3的化学性质反应前后没有改变.
【拓展】下表是同学们探究影响H2O2分解因素时所记录的部分数据:
用足量等体积H2O2溶液制取相同体积O2所需时间
通过对表格中的数据进行分析,你能得出的结论是相同条件下,MnO2的催化效果比Fe2O3好.
【延伸】小明同学看到Fe2O3也能做H2O2分解的催化剂,还联想到一种蓝色的CuSO4溶液也能做H2O2分解的催化剂,请你一起参与计算:
(1)CuSO4的相对分子质量160;
(2)80g CuSO4中铜元素的质量?(写出计算过程)
【猜想】Fe2O3能否作为H2O2分解的催化剂.
【实验验证】小丽同学一次设计了三个实验
实验一 取一定量的H2O2溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,观察到木条没有复燃,说明H2O2溶液常温下分解缓慢.
实验二 在实验一的试管中加入wg Fe2O3粉末,有大量气泡产生,然后伸入带火星的木条,观察到木条复燃,说明Fe2O3能加快H2O2的分解速率.
实验三 待反应结束后,将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为wg,说明反应前后Fe2O3的质量保持不变.
【实验结论】小丽同学认为,Fe2O3粉末可以作为H2O2分解的催化剂.
【反思评价】小江同学认为要证明小丽同学的结论正确,仅做这三个实验还不充分,需要补充一个探究实验,探究Fe2O3的化学性质反应前后没有改变.
【拓展】下表是同学们探究影响H2O2分解因素时所记录的部分数据:
用足量等体积H2O2溶液制取相同体积O2所需时间
| 浓度 时间/min 催化剂 | 30% H2O2 溶液 | 15% H2O2 溶液 | 5% H2O2 溶液 |
| 加入wg MnO2 | 0.2 | 0.8 | 2.0 |
| 加入wg Fe2O3 | 7.0 | 9.0 | 16.0 |
【延伸】小明同学看到Fe2O3也能做H2O2分解的催化剂,还联想到一种蓝色的CuSO4溶液也能做H2O2分解的催化剂,请你一起参与计算:
(1)CuSO4的相对分子质量160;
(2)80g CuSO4中铜元素的质量?(写出计算过程)
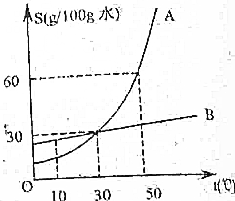 如图是A、B两种固体的溶解度曲线,请回答下列问题
如图是A、B两种固体的溶解度曲线,请回答下列问题