题目内容
下列关于溶解度的叙述中,正确的是( )
①将36g NaCl溶于100g水中制成饱和溶液,NaCl的溶解度为36g. ②20℃时,100克NaCl饱和溶液中含有26.5克NaCl,因此,NaCl在20℃时的溶解度为26.5克.③在20℃时,100克水最多能溶解31.6克KNO3,而200克水最多能溶解63.2克KNO3,因此,KNO3的溶解度随溶剂质量增大而增大. ④在20℃时,100克水中溶解了NaCl 20克,因此NaCl在20℃时的溶解度为20g.⑤在20℃时,NaCl的溶解度为36克. ⑥在20℃时,100克水中溶解36克NaCl达到饱和状态,因此,NaCl在20℃的溶解度为解度为36克.
①将36g NaCl溶于100g水中制成饱和溶液,NaCl的溶解度为36g. ②20℃时,100克NaCl饱和溶液中含有26.5克NaCl,因此,NaCl在20℃时的溶解度为26.5克.③在20℃时,100克水最多能溶解31.6克KNO3,而200克水最多能溶解63.2克KNO3,因此,KNO3的溶解度随溶剂质量增大而增大. ④在20℃时,100克水中溶解了NaCl 20克,因此NaCl在20℃时的溶解度为20g.⑤在20℃时,NaCl的溶解度为36克. ⑥在20℃时,100克水中溶解36克NaCl达到饱和状态,因此,NaCl在20℃的溶解度为解度为36克.
| A、①②④ | B、②⑥ |
| C、③④⑤⑥ | D、⑤⑥ |
考点:固体溶解度的概念
专题:溶液、浊液与溶解度
分析:根据固体溶解度的概念进行判断.
解答:解:①将36g NaCl溶于100g水中制成饱和溶液,没有指明温度,故不知该温度下的溶解度.故①错误;
②20℃时,应该是100克溶剂中含有26.5克NaCl的饱和溶液.故②错误;
③在20℃时,KNO3的溶解度是31.6克,没有变化.故③错误;
④在20℃时,100克水中溶解了NaCl 20克,不知该溶液是否为饱和溶液,无法计算其溶解度.故④错误;
⑤在20℃时,NaCl的溶解度为36克.故⑤正确;
⑥在20℃时,100克水中溶解36克NaCl达到饱和状态,则溶解度是36克.故⑥正确.
故选:D.
②20℃时,应该是100克溶剂中含有26.5克NaCl的饱和溶液.故②错误;
③在20℃时,KNO3的溶解度是31.6克,没有变化.故③错误;
④在20℃时,100克水中溶解了NaCl 20克,不知该溶液是否为饱和溶液,无法计算其溶解度.故④错误;
⑤在20℃时,NaCl的溶解度为36克.故⑤正确;
⑥在20℃时,100克水中溶解36克NaCl达到饱和状态,则溶解度是36克.故⑥正确.
故选:D.
点评:固体溶解度的概念是指在一定的温度下,某物质在100克溶剂里达到饱和状态时所溶解的质量.

练习册系列答案
相关题目
“盐是人体正常生理活动必不可少的物质”.这里的盐是指( )
| A、Na2CO3 |
| B、NaCl |
| C、CuSO4 |
| D、CaCO3 |
密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:
已知X的相对分子质量为n,Q的相对分子质量为2n,下列推断正确的是( )
| 物 质 | X | Y | Z | Q |
| 反应前质量/g | 4 | 10 | 1 | 21 |
| 反应后质量/g | 0 | 12 | 15 | 待测 |
| A、反应后Q的质量为9 g |
| B、反应后生成15 gZ |
| C、反应中Y与Q发生改变的质量比为1:1 |
| D、该反应方程式中X与Q的化学计量数之比为2:3 |
能用浓H2SO4干燥,又能用固体NaOH干燥的气体是( )
①SO2 ②NH3 ③CO2 ④H2 ⑤O2.
①SO2 ②NH3 ③CO2 ④H2 ⑤O2.
| A、①③ | B、④⑤ |
| C、①②③ | D、①④⑤ |
下列说法中正确的是( )
| A、食盐与水混合得到食盐水属于化合反应 |
| B、有氧气参加的反应一定是化合反应 |
| C、化合反应可能是物理变化 |
| D、氧化反应一定是化学变化 |
下列物质在氧气中燃烧时,集气瓶内需要预先加入少量水或细沙的是( )
| A、硫磺 | B、铁丝 | C、木炭 | D、铝箔 |
下列说法中错误的是( )
| A、有氧气参与的反应一定是氧化反应 |
| B、催化剂一定能加快反应速率 |
| C、化合反应中反应物至少有两种 |
| D、分解反应中反应物只有一种 |
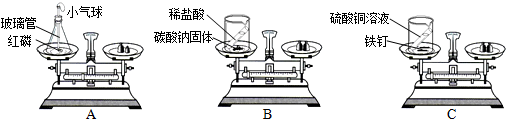



 已知空气的主要成分示氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图:
已知空气的主要成分示氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图: