题目内容
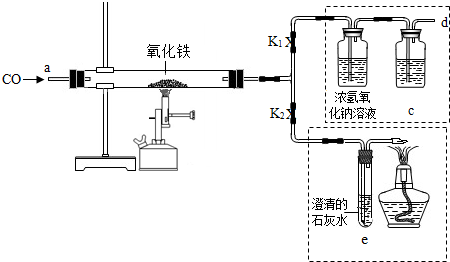
某校学生要进行一系列的实验,请结合如图帮助他们解决以下问题:

(1)图中标有①的仪器名称为:
(2)用加热高锰酸钾的方法制取氧气,应选用的发生装置是 (填字母编号),
(3)实验室制取氢气,选用的收集装置为 (填字母编号).
(4)用B、D装置可制取某种能使石灰水变浑浊的气体,制取该气体的化学方程式为 .
(5)已知浓盐酸具有挥发性,易挥发出氯化氢气体.浓盐酸和大理石在B装置中混合剧烈反应,将放出的气体M直接通入澄清石灰水中,石灰水没有变浑浊.
据此事实估计,该气体M中应含有 等成分.
(6)实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水.
①该反应的化学方程式是.收集氨气时应选用E装置,把收集满氨气的集气瓶倒扣在滴有无色酚酞试液的水槽中,观察到集气瓶内有大量红色液体进入.
②根据上述信息总结出氨气的性质有(至少答2条) .

(1)图中标有①的仪器名称为:
(2)用加热高锰酸钾的方法制取氧气,应选用的发生装置是
(3)实验室制取氢气,选用的收集装置为
(4)用B、D装置可制取某种能使石灰水变浑浊的气体,制取该气体的化学方程式为
(5)已知浓盐酸具有挥发性,易挥发出氯化氢气体.浓盐酸和大理石在B装置中混合剧烈反应,将放出的气体M直接通入澄清石灰水中,石灰水没有变浑浊.
据此事实估计,该气体M中应含有
(6)实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水.
①该反应的化学方程式是.收集氨气时应选用E装置,把收集满氨气的集气瓶倒扣在滴有无色酚酞试液的水槽中,观察到集气瓶内有大量红色液体进入.
②根据上述信息总结出氨气的性质有(至少答2条)
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,氢气的制取和检验,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)从仪器的图形和用途去分析解答;
(2)从用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,反应需要加热去分析解答;
(3)从氢气不溶于水,故可用排水法收集F;又由于密度比空气小,故可以用E向下排空气法进行收集,去分析解答;
(4)从能使石灰水变浑浊的气体是二氧化碳,实验室里用大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl)制取二氧化碳,二者接触即可发生反应生成氯化钙、水和二氧化碳去分析解答;
(5)从①由于反应物有浓盐酸和大理石,二者反应生成二氧化碳;②同时由于浓盐酸中水分,故产生的气体中还含有水蒸气;③题目中指出:“放出的气体M直接通入澄清石灰水中,石灰水没有变浑浊.”说明二氧化碳和石灰水反应生成的碳酸钙被氯化氢气体溶于水形成的盐酸溶解,说明气体M中含有浓盐酸挥发出的氯化氢气体去分析解答;
(6)从①实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水,由此可知反应物是氯化铵和氢氧化钙,生成物是氯化钙、水的氨气,去分析解答;
②从收集氨气时应选用向下排空气法(E装置)可知氨气的密度比空气小;把收集满氨气的集气瓶倒扣在滴有无色酚酞试液的水槽中,观察到集气瓶内有大量液体进入说明氨气极溶于水;溶液变成红色(无色酚酞溶液遇碱变红),说明氨气的水溶液呈碱性去分析解答.
(2)从用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,反应需要加热去分析解答;
(3)从氢气不溶于水,故可用排水法收集F;又由于密度比空气小,故可以用E向下排空气法进行收集,去分析解答;
(4)从能使石灰水变浑浊的气体是二氧化碳,实验室里用大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl)制取二氧化碳,二者接触即可发生反应生成氯化钙、水和二氧化碳去分析解答;
(5)从①由于反应物有浓盐酸和大理石,二者反应生成二氧化碳;②同时由于浓盐酸中水分,故产生的气体中还含有水蒸气;③题目中指出:“放出的气体M直接通入澄清石灰水中,石灰水没有变浑浊.”说明二氧化碳和石灰水反应生成的碳酸钙被氯化氢气体溶于水形成的盐酸溶解,说明气体M中含有浓盐酸挥发出的氯化氢气体去分析解答;
(6)从①实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水,由此可知反应物是氯化铵和氢氧化钙,生成物是氯化钙、水的氨气,去分析解答;
②从收集氨气时应选用向下排空气法(E装置)可知氨气的密度比空气小;把收集满氨气的集气瓶倒扣在滴有无色酚酞试液的水槽中,观察到集气瓶内有大量液体进入说明氨气极溶于水;溶液变成红色(无色酚酞溶液遇碱变红),说明氨气的水溶液呈碱性去分析解答.
解答:解:(1)由仪器的图形和用途可知仪器为长颈漏斗,故答案为:长颈漏斗;
(2)用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,所以化学方程式为:2KMnO4
K2MnO4+MnO2+O2↑;由于反应需要加热,所以发生装置选择A;故答案为A;
(3)由于收集的氢气不溶于水,故可用排水法收集F;又由于密度比空气小,故可以用E向下排空气法进行收集,故答案为:E或F;
(4)能使石灰水变浑浊的气体是二氧化碳,实验室里用大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl)制取二氧化碳,二者接触即可发生反应生成氯化钙、水和二氧化碳.其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(5)浓盐酸和大理石在B装置中混合剧烈反应,将放出的气体M,①由于反应物有浓盐酸和大理石,二者反应生成二氧化碳;②同时由于浓盐酸中水分,故产生的气体中还含有水蒸气;③题目中指出:“放出的气体M直接通入澄清石灰水中,石灰水没有变浑浊.”说明二氧化碳和石灰水反应生成的碳酸钙被氯化氢气体溶于水形成的盐酸溶解,说明气体M中含有浓盐酸挥发出的氯化氢气体;故答案为:HCl、CO2、水蒸气;
(6)①实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水,由此可知反应物是氯化铵和氢氧化钙,生成物是氯化钙、水的氨气,故化学方程式为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
②收集氨气时应选用向下排空气法(E装置)可知氨气的密度比空气小;把收集满氨气的集气瓶倒扣在滴有无色酚酞试液的水槽中,观察到集气瓶内有大量液体进入说明氨气极溶于水;溶液变成红色(无色酚酞溶液遇碱变红),说明氨气的水溶液呈碱性;故答案为:氨气的密度比空气小、氨气易溶于水、氨气的水溶液呈碱性.
(2)用加热高锰酸钾的方法制取氧气,在生成氧气的同时,还有锰酸钾和二氧化锰生成,所以化学方程式为:2KMnO4
| ||
(3)由于收集的氢气不溶于水,故可用排水法收集F;又由于密度比空气小,故可以用E向下排空气法进行收集,故答案为:E或F;
(4)能使石灰水变浑浊的气体是二氧化碳,实验室里用大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl)制取二氧化碳,二者接触即可发生反应生成氯化钙、水和二氧化碳.其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(5)浓盐酸和大理石在B装置中混合剧烈反应,将放出的气体M,①由于反应物有浓盐酸和大理石,二者反应生成二氧化碳;②同时由于浓盐酸中水分,故产生的气体中还含有水蒸气;③题目中指出:“放出的气体M直接通入澄清石灰水中,石灰水没有变浑浊.”说明二氧化碳和石灰水反应生成的碳酸钙被氯化氢气体溶于水形成的盐酸溶解,说明气体M中含有浓盐酸挥发出的氯化氢气体;故答案为:HCl、CO2、水蒸气;
(6)①实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(NH3),同时得到氯化钙和水,由此可知反应物是氯化铵和氢氧化钙,生成物是氯化钙、水的氨气,故化学方程式为:2NH4Cl+Ca(OH)2
| ||
| ||
②收集氨气时应选用向下排空气法(E装置)可知氨气的密度比空气小;把收集满氨气的集气瓶倒扣在滴有无色酚酞试液的水槽中,观察到集气瓶内有大量液体进入说明氨气极溶于水;溶液变成红色(无色酚酞溶液遇碱变红),说明氨气的水溶液呈碱性;故答案为:氨气的密度比空气小、氨气易溶于水、氨气的水溶液呈碱性.
点评:理解气体的收集方法取决于气体的密度和水溶性.

练习册系列答案
相关题目
下列物质的用途中,主要利用其化学性质的是( )
| A、钢材可以做铁轨 |
| B、稀有气体可用做霓虹灯 |
| C、氧气可以支持燃烧 |
| D、钻石可用来做漂亮的装饰品 |
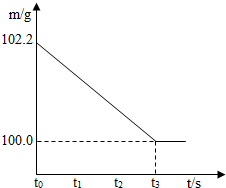 将碳酸钠和硫酸钠的固体混合物12.2g放入烧杯中,再加入一定质量的稀硫酸使其恰好反应,测得反应后所得溶液中溶质质量分数为17.5%,烧杯和所盛物质的总质量(m)与反应时间(t)的关系如图所示.计算:
将碳酸钠和硫酸钠的固体混合物12.2g放入烧杯中,再加入一定质量的稀硫酸使其恰好反应,测得反应后所得溶液中溶质质量分数为17.5%,烧杯和所盛物质的总质量(m)与反应时间(t)的关系如图所示.计算: