题目内容
8.硫酸、盐酸是重要的化工原料.(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有吸水性.
(2)写出下列反应的化学方程式:
①用熟石灰中和硫酸厂排出的废水Ca(OH)2+H2SO4═CaSO4+2H2O
②将生锈铁钉加入稀硫酸中一段时间后铁锈消失铁钉表面有气泡:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;Fe+H2SO4═FeSO4+H2↑.
③稀硫酸与碳酸钠溶液反应:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是②③(填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH.
分析 (1)根据浓硫酸具有吸水性,进行分析解答.
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
(3)根据盐酸、硫酸都能与金属氧化物反应;通常制作氯化锌用盐酸;除杂不得引入新的杂质,进行分析解答.
解答 解:(1)硫酸在实验室常用作干燥剂,因为浓硫酸有吸水性.
(2)①熟石灰与稀硫酸反应生成硫酸钙和水,反应的化学方程式为:Ca(OH)2+H2SO4═CaSO4+2H2O.
②铁锈的主要成分是氧化铁,与硫酸反应生成硫酸铁和水,反应的化学方程式是:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;铁与稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑.
③稀硫酸与碳酸钠溶液反应生成硫酸钠、水和二氧化碳,反应的化学方程式为:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.
(3)①稀盐酸、稀硫酸均可用于金属表面除锈.
②硫酸中不含氯元素,不用硫酸作为制取药物氯化锌.
③氢氧化钠与稀硫酸反应生成硫酸钠和水,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则.
故答案为:(1)吸水;(2)①Ca(OH)2+H2SO4═CaSO4+2H2O;②Fe2O3+3H2SO4═Fe2(SO4)3+3H2O、Fe+H2SO4═FeSO4+H2↑;③Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;(3)②③.
点评 本题难度不大,掌握酸的化学性质、浓硫酸具有吸水性、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
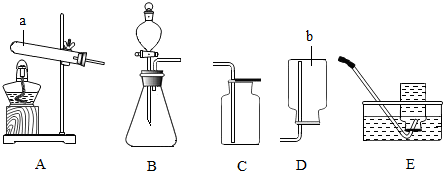
3.根据下列实验装置图,回答问题.
(1)写出图中仪器的名称:a长颈漏斗b集气瓶.
(2)实验室用加热氯酸钾和二氧化锰的混合物制取氧气,该反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,可选择的发生装置为A(填字母).
(3)实验室常用石灰石和稀盐酸反应制取二氧化碳,可以用D装置收集二氧化碳的原因是二氧化碳的密度大于空气的密度.
(4)如果通过F装置干燥气体,则F装置盛有的试剂为浓硫酸.
| 发生装置 | 收集装置 | 洗气装置 |
 |  |  |
(2)实验室用加热氯酸钾和二氧化锰的混合物制取氧气,该反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,可选择的发生装置为A(填字母).
(3)实验室常用石灰石和稀盐酸反应制取二氧化碳,可以用D装置收集二氧化碳的原因是二氧化碳的密度大于空气的密度.
(4)如果通过F装置干燥气体,则F装置盛有的试剂为浓硫酸.
 右下示意图形象地表示了某化学反应前后分子的变化.其中
右下示意图形象地表示了某化学反应前后分子的变化.其中 表示氧原子、
表示氧原子、 表示碳原子,该反应的化学方程式为:
表示碳原子,该反应的化学方程式为: