题目内容
1.从氧气、二氧化碳、水蒸气、氮气、稀有气体等五种气体中,选择适当的物质填空.(1)燃料的燃烧离不开的是氧气;(2)用于食品防腐的是氮气;
(3)能使澄清石灰水变浑浊的是二氧化碳;(4)会使香脆的瓜子变软的是水蒸气;
(5)用于霓虹灯的是稀有气体.
分析 根据各种气体的性质和用途进行分析解答;
解答 解:(1)氧气能助燃,燃料的燃烧离不开,故填:氧气;
(2)氮气性质稳定,无毒,常用于食品防腐,故填:氮气;
(3)二氧化碳能使澄清的石灰水变浑浊;故填:二氧化碳;
(4)香脆的瓜子会吸收空气中的水蒸气而变软;故填:水蒸气;
(5)稀有气体通电后能发出各种颜色的光,常用于制霓虹灯;故填:稀有气体;
点评 本题考查气体的性质和用途,物质的性质决定物质的用途,学习中要牢记.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.酸、碱、盐是几类重要的化合物,他们之间能发生复分解反应.
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有水生成.
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象.取反应后的部分溶液加热、蒸干、得到白色固体.
以下是探究白色固体成分的实验,已知CaCl2溶液呈中性.请填写下表:
实验反思:无明显现象的中和反应可借助酸碱指示剂判断反应终点.
(3)“粗盐提纯”指除去NaCl中的泥沙和MgCl2、CaCl2、Na2SO4等杂质.
某同学设计了除去三种可溶性杂质的实验方案:先将固体溶解,然后向其中依次加入过量的BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,蒸发结晶.请回答:
部分物质的溶解性表(室温)
①溶解、过滤和蒸发操作中都用到一种玻璃仪器,该仪器在蒸发操作中的作用是什么?
②加入Na2CO3溶液的目的是什么?
③以上方案还需完善,请说明原因并加以补充.
(4)LiOH和NaOH的化学性质相似.“神舟”飞船内,可用盛有LiOH的过滤网吸收航天员呼出的气体,以降低CO2含量.请计算:用LiOH完全吸收176gCO2生成Li2CO3和H2O,理论上至少需要LiOH的质量是多少?
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有水生成.
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象.取反应后的部分溶液加热、蒸干、得到白色固体.
以下是探究白色固体成分的实验,已知CaCl2溶液呈中性.请填写下表:
| 实验操作 | 测定结果 | 白色固体成分 |
| 用pH试纸测定反应后溶液的酸碱度,操作方法是 用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较 | pH>7 | |
| pH=7 | CaCl2 |
(3)“粗盐提纯”指除去NaCl中的泥沙和MgCl2、CaCl2、Na2SO4等杂质.
某同学设计了除去三种可溶性杂质的实验方案:先将固体溶解,然后向其中依次加入过量的BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,蒸发结晶.请回答:
部分物质的溶解性表(室温)
| OH- | Cl- | SO42- | CO32- | |
| H+ | 溶、挥 | 溶 | 溶、挥 | |
| Ba2+ | 溶 | 溶 | 不溶 | 不溶 |
| Ca2+ | 微溶 | 溶 | 微溶 | 不溶 |
| Mg2+ | 不溶 | 溶 | 溶 | 微溶 |
②加入Na2CO3溶液的目的是什么?
③以上方案还需完善,请说明原因并加以补充.
(4)LiOH和NaOH的化学性质相似.“神舟”飞船内,可用盛有LiOH的过滤网吸收航天员呼出的气体,以降低CO2含量.请计算:用LiOH完全吸收176gCO2生成Li2CO3和H2O,理论上至少需要LiOH的质量是多少?
9.实验室中区分下列各组物质的两种方法都正确的是( )
| 选项 | 需要区分的物质 | 实验方法 |
| A | 磷酸钙和氯化铵 | ①闻气味 ②与熟石灰混合研磨 |
| B | 氯化钠和硝酸钾 | ①加水溶解测温度 ②测其溶液的导电性 |
| C | 氢氧化钾溶液和碳酸钠溶液 | ①滴加稀硝酸 ②滴加氯化钙 |
| D | 硬水和软水 | ①加肥皂水 ②取水样加热、煮沸 |
| A. | A | B. | B | C. | C | D. | D |
16.6月5日是世界环境日,环境保护是我国的一项基本国策,空气的净化越来越受到人们的关注,下列不会造成空气污染的是( )
| A. | 燃油机排放的尾气 | B. | 露天焚烧垃圾 | ||
| C. | 植物的光合作用 | D. | 煤燃烧排放出的烟气 |

 表示:氧原子
表示:氧原子 表示;氢原子
表示;氢原子  表示:氯原子
表示:氯原子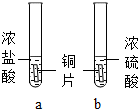 化学课上探究金属的化学性质时,同学们发现铜与稀盐酸、稀硫酸在常温或短时间加热的条件下均不反应.那么,铜与浓盐酸、浓硫酸能否发生反应呢?兴趣小组进行如下探究.
化学课上探究金属的化学性质时,同学们发现铜与稀盐酸、稀硫酸在常温或短时间加热的条件下均不反应.那么,铜与浓盐酸、浓硫酸能否发生反应呢?兴趣小组进行如下探究.