题目内容
15.对物质进行分类,是研究物质的基本方法.在下面的四种化合物中,与另外三种不属于同一类别的物质是( )| A. | HC1 | B. | NaCl | C. | Na2CO3 | D. | FeSO4•7H2O |
分析 根据化合物中的酸是指电离时生成的阳离子全部是氢离子的化合物,盐是指由金属离子和酸根离子组成的化合物进行分析.
解答 解:A、HCl是电离时生成的阳离子全部是氢离子的化合物,属于酸;
B、NaCl是由钠离子和氯离子组成的化合物,属于盐;
C、Na2CO3是由钠离子和碳酸根离子构成的化合物,属于盐;
D、FeSO4•7H2O是由金属离子和酸根离子组成的化合物,属于盐.
故选:A.
点评 解答本题要掌握物质的分类方法,只有这样才能对各种物质进行正确的分类,难度不大.

练习册系列答案
相关题目
5.下列是几种典型物质与氧气发生反应时实验现象的描述,其中正确的是( )
| A. | 木炭在空气中燃烧既发红又发出白光 | |
| B. | 红磷在氧气中燃烧产生大量白雾 | |
| C. | 细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 硫在空气中燃烧发出蓝紫色火焰,生成一种无色无味气体 |
20.下列四个坐标示意图分别表示四个实验过程中的某些变化情况,其中错误的是( )


| A. | 在一定质量表面被氧化的镁条中,慢慢加入一定浓度的盐酸,产生MgCl2质量变化 | |
| B. | 等质量的镁条和铁丝分别与足量的稀硫酸反应,产生气体的质量变化 | |
| C. | 向一定量的二氧化锰固体中加入一定量的过氧化氢溶液,二氧化锰的质量变化 | |
| D. | 将水通电一段时间,相同状况下产生气体的体积变化 |
7. 欲测定铜镁合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下:
欲测定铜镁合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下:
(l)m的值是14,合金中铜、镁的质量最简比是7:3;
(2)用第1次实验的数据计算所加稀硫酸的溶质的质量分数;(写出计算过程)
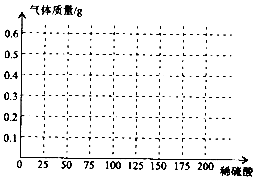
(3)在如图画出加入稀硫酸与产生气体关系的曲线图.
 欲测定铜镁合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下:
欲测定铜镁合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金20g放入烧杯,将200g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下:| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 17.6 | 15.2 | m | 14 |
(2)用第1次实验的数据计算所加稀硫酸的溶质的质量分数;(写出计算过程)
(3)在如图画出加入稀硫酸与产生气体关系的曲线图.


 (4)下列说法错误的是③(填序号).
(4)下列说法错误的是③(填序号).