题目内容
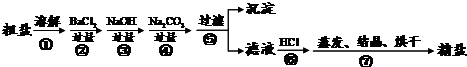
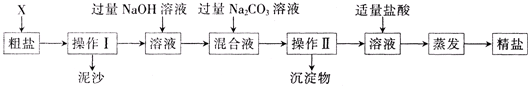
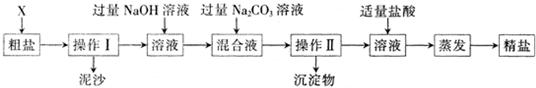
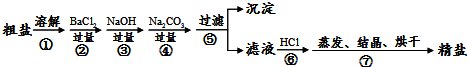
通过海水晾晒可得粗盐,粗盐除NaCI外,还含.有MgCI2、CaCI2、Na2SO4以及泥沙等杂质:以下是制备精盐的实验方案,各步操作流程如下:
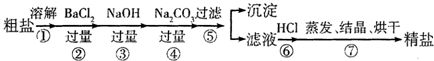
(1)在第⑦步滤液蒸发中要用玻璃棒搅拌,目的是______.
(2)第②步操作的目的是除去粗盐中的______(填化学式,下同)第⑥步操作的目的是除去滤液中的______.
(3)第⑤步“过滤”操作中得到的沉淀,除了有泥沙、CaCO3、BaSO4、Mg(OH)2外,还有______. (填物质的化学式):
(4)在第③步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是______.
解:(1)在第⑦步滤液蒸发中要用玻璃棒搅拌,目的是防止液体局部沸腾,造成液滴飞溅.
故填:防止液体局部沸腾,造成液滴飞溅.
(2)第②步操作的目的是除去粗盐中的硫酸钠,硫酸钠的化学式是Na2SO4;第⑥步操作的目的是除去滤液中过量的碳酸钠和氢氧化钠,化学式分别是Na2CO3、NaOH.
故填:Na2SO4;Na2CO3、NaOH.
(3)第⑤步“过滤”操作中得到的沉淀,除了有泥沙、CaCO3、BaSO4、Mg(OH)2外,还有碳酸钡,化学式是BaCO3.
故填:BaCO3.
(4)不能用KOH代替NaOH,理由是:氢氧化钾和氯化镁反应能生成氢氧化镁沉淀和氯化钾,会引入新杂质氯化钾.
故填:会引入新杂质氯化钾.
分析:向溶液中加入过量的氯化钡时,氯化钡能和硫酸钠反应生成硫酸钡沉淀和氯化钠,从而除去硫酸钠;
加入过量的氢氧化钠溶液时,氢氧化钠能和氯化镁反应生成氢氧化镁沉淀和氯化钠,从而除去氯化镁;
加入过量的碳酸钠溶液时,碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠,能和过量的氯化钡反应生成碳酸钡沉淀和氯化钠,从而除去氯化钙和剩余的氯化钡;
加入稀盐酸时,稀盐酸能和氢氧化钠反应生成氯化钠和水,能和碳酸钠反应生成氯化钠、水和二氧化碳,从而除去过量的氢氧化钠和碳酸钠.
点评:化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.
故填:防止液体局部沸腾,造成液滴飞溅.
(2)第②步操作的目的是除去粗盐中的硫酸钠,硫酸钠的化学式是Na2SO4;第⑥步操作的目的是除去滤液中过量的碳酸钠和氢氧化钠,化学式分别是Na2CO3、NaOH.
故填:Na2SO4;Na2CO3、NaOH.
(3)第⑤步“过滤”操作中得到的沉淀,除了有泥沙、CaCO3、BaSO4、Mg(OH)2外,还有碳酸钡,化学式是BaCO3.
故填:BaCO3.
(4)不能用KOH代替NaOH,理由是:氢氧化钾和氯化镁反应能生成氢氧化镁沉淀和氯化钾,会引入新杂质氯化钾.
故填:会引入新杂质氯化钾.
分析:向溶液中加入过量的氯化钡时,氯化钡能和硫酸钠反应生成硫酸钡沉淀和氯化钠,从而除去硫酸钠;
加入过量的氢氧化钠溶液时,氢氧化钠能和氯化镁反应生成氢氧化镁沉淀和氯化钠,从而除去氯化镁;
加入过量的碳酸钠溶液时,碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠,能和过量的氯化钡反应生成碳酸钡沉淀和氯化钠,从而除去氯化钙和剩余的氯化钡;
加入稀盐酸时,稀盐酸能和氢氧化钠反应生成氯化钠和水,能和碳酸钠反应生成氯化钠、水和二氧化碳,从而除去过量的氢氧化钠和碳酸钠.
点评:化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
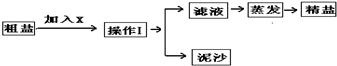
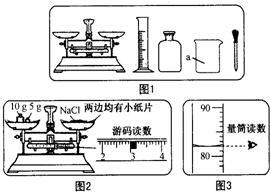 某实验小组利用图1所示仪器进行“配制质量分数一定的氯化钠溶液”的实验:
某实验小组利用图1所示仪器进行“配制质量分数一定的氯化钠溶液”的实验: