题目内容
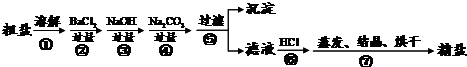
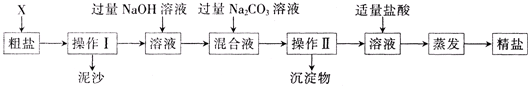
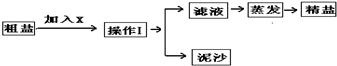
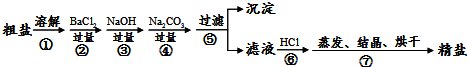
35、通过海水晾晒可得粗盐.粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质.为了有效将粗盐提纯,实验的各步操作流程如下图所示.根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的X物质是
(2)操作Ⅰ和操作Ⅱ的名称是
(3)在实验过程中加入过量的NaOH溶液,其实验目的是
(4)判断加入的盐酸“适量”的方法是
(5)实验所得精盐的质量大于粗盐中NaCl的质量,原因是
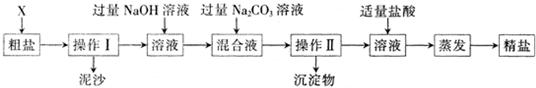
(1)在完成操作Ⅰ之前,必须加入的X物质是
水
.(2)操作Ⅰ和操作Ⅱ的名称是
过滤
.(3)在实验过程中加入过量的NaOH溶液,其实验目的是
除掉镁离子使其转化成沉淀
,有关化学方程式是MgCl2+2NaOH═Mg(OH)2↓+2NaCl
.(4)判断加入的盐酸“适量”的方法是
滴加盐酸无气泡放出为适宜
.(5)实验所得精盐的质量大于粗盐中NaCl的质量,原因是
在粗盐提纯的过程中有氯化钠生成.
.
分析:(1)根据粗盐的提纯需要将其配成溶液才能进行,
(2)分离固体与溶液的方法是过滤,
(3)氢氧化钠可以将水中的镁离子转化为沉淀而得到净水的目的,
(4)盐酸与碳酸钠反应是有气泡产生.
(5)在提纯过程中生成了氯化钠.
(2)分离固体与溶液的方法是过滤,
(3)氢氧化钠可以将水中的镁离子转化为沉淀而得到净水的目的,
(4)盐酸与碳酸钠反应是有气泡产生.
(5)在提纯过程中生成了氯化钠.
解答:解:
(1)海水晾晒得到的粗盐是固体,要进行提纯,需要先配成溶液,
故答案为:水.
(2)分离固体与溶液的方法是过滤,I、II都是分理处沉淀的过程.
故答案为:过滤.
(3)加入过量的氢氧化钠,氢氧根离子可以和镁离子转化为氢氧化镁沉淀而将镁离子除去.
故答案为:将镁离子全部沉淀;MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
(4)此步是除掉多余的碳酸钠,而盐酸与碳酸钠反应是有气泡产生,从现象即可判断.
故答案为:滴加盐酸无气泡放出为适宜.
(5)在粗盐提纯的过程中,在提纯过程中生成了氯化钠.所以实验所得精盐的质量大于粗盐中NaCl的质量.
故答案为:在粗盐提纯的过程中有氯化钠生成.
(1)海水晾晒得到的粗盐是固体,要进行提纯,需要先配成溶液,
故答案为:水.
(2)分离固体与溶液的方法是过滤,I、II都是分理处沉淀的过程.
故答案为:过滤.
(3)加入过量的氢氧化钠,氢氧根离子可以和镁离子转化为氢氧化镁沉淀而将镁离子除去.
故答案为:将镁离子全部沉淀;MgCl2+2NaOH═Mg(OH)2↓+2NaCl.
(4)此步是除掉多余的碳酸钠,而盐酸与碳酸钠反应是有气泡产生,从现象即可判断.
故答案为:滴加盐酸无气泡放出为适宜.
(5)在粗盐提纯的过程中,在提纯过程中生成了氯化钠.所以实验所得精盐的质量大于粗盐中NaCl的质量.
故答案为:在粗盐提纯的过程中有氯化钠生成.
点评:本题考查了物质的除杂的有关问题,难度比较大,特别的除去食盐中的多种杂质,要根据除杂的原理深入思考,按照最优化的顺序添加除杂剂.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
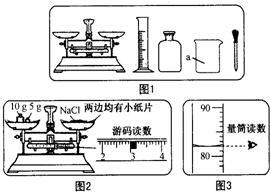 某实验小组利用图1所示仪器进行“配制质量分数一定的氯化钠溶液”的实验:
某实验小组利用图1所示仪器进行“配制质量分数一定的氯化钠溶液”的实验: