题目内容
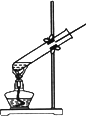
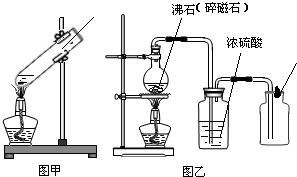
某化学兴趣小组同学在实验中发现,用下图甲所示装置加热质量分数为10%H2O2溶液制O2,用带火星的木条检验时,木条不复燃.
[猜想]同学们经过认真分析,猜想其可能的原因
根据可燃物在纯氧中燃烧比在空气中燃烧剧烈,第一组同学认为:________;
第二组认为:________.
[实验验证]各组同学经过热烈讨论,结合猜想制定了每组的实验方案并进行了实验.
(1)第一组同学用下图装置,加热质量分数为15%的H2O2溶液,用带火星的木条检验O2,木条不复燃.
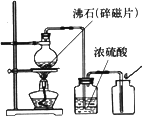
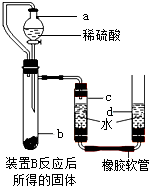
(2)第二组同学从实验装置上进行了改进(见下图).用10%的H2O2溶液进行实验,木条复燃.使用该装置在停止加热时,要进行的操作是________.
[得出结论]在实验基础上,同学们经过讨论,得出了一些结论.
(1)第一组同学认为:增大反应物的浓度不能加快化学反应速率.你是否同意他们的说法(填“是”或“否”)_______.
(2)第二组同学的实验验证了他们猜想的正确性.
经过进一步实验探究,同学们最终选择在常温下向H2O2溶液中加入少量二氧化锰固体粉末来制O2,该反应的化学方程式为________,其中二氧化锰所起的作用是________.
答案:
解析:
解析:
|
[猜想]第一组:过氧化氢溶液浓度太低,使分解产生氧气缓慢(或产生氧气量少) 第二组:过氧化氢分解产生的氧气中含有水蒸气 [实验验证](2)先将导气管从浓硫酸中取出,再熄灭酒精灯 [得出结论](1)否 2H2O2 |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
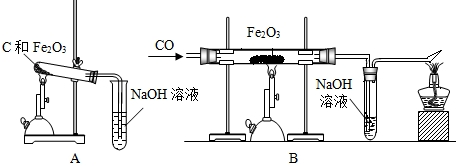
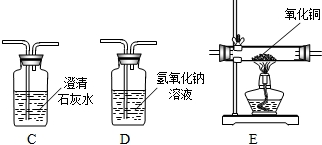
 .
. 铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.图1是稀释浓硫酸实验的示意图.
铝、铁、铜是人类广泛使用的三种金属,与我们生活息息相关.图1是稀释浓硫酸实验的示意图. 已知M、N分别是稀硫酸、氢氧化钠溶液中的一种.某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH,如图所示.
已知M、N分别是稀硫酸、氢氧化钠溶液中的一种.某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH,如图所示.