题目内容
2.如图中的①、②分别是钠元素、;氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图.
试回答下列问题:
(1)钠元素的原子序数为11.
(2)A、B、C中属于同种元素的粒子是B和C,具有相对稳定结构的是C.(用字母序号填空)
(3)A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质;
(4)钠原子和氯原子反应所形成的化合物是由离子(填“分子”、“原子”、“离子”)构成的.
分析 (1)左上角数字属于原子序数;(2)决定元素种类的是质子数或核电荷数,最外层电子数是8(一个电子层的是2)属于稳定结构;(3)决定元素化学性质的是最外层电子数;(4)氯化钠是由钠离子和氯离子构成.
解答 解:(1)左上角数字属于原子序数,钠元素的原子序数为11;
(2)决定元素种类的是质子数或核电荷数,所以A、B、C中属于同种元素的粒子是B和C;最外层电子数是8(一个电子层的是2)属于稳定结构,所以具有相对稳定结构的是C;
(3)决定元素化学性质的是最外层电子数,A和B两种粒子的最外层电子数相等,所以化学性质相似;
(4)钠原子最外层电子数是1,容易失去一个电子变成钠离子,氯元素最外层电子数是7,容易得到一个电子,变成氯离子,所以氯化钠是由钠离子和氯离子构成.
故答案为:(1)11;(2)B和C;C;(3)最外层电子数;(4)离子.
点评 本题考查学生根据1869年以门捷列夫为代表的科学家发现了元素周期表,原子序数概念,原子序数=质子数,决定元素种类的是质子数或核电荷数,决定元素化学性质的是最外层电子数.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
11.氨碱法生产纯碱的主要反应原理如下:
(1)NaCl+NH3+CO2+H20═NaHCO3+NH4Cl
(2)2NaHCO3$\frac{\underline{\;加热\;}}{\;}$Na2CO3+CO2↑+H2O.
对上述信息的有关理解不正确的是( )
(1)NaCl+NH3+CO2+H20═NaHCO3+NH4Cl
(2)2NaHCO3$\frac{\underline{\;加热\;}}{\;}$Na2CO3+CO2↑+H2O.
对上述信息的有关理解不正确的是( )
| A. | 用食盐制纯碱需要含碳、氧元素的物质 | |
| B. | (1)中析出晶体后剩余溶液只有一种溶质 | |
| C. | 氨盐水比食盐水更易吸收二氧化碳 | |
| D. | 碳酸氢钠比碳酸钠受热更易分解 |
12.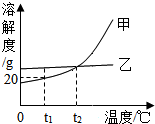 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )| A. | 甲的溶解度比乙大 | |
| B. | t2℃时,甲、乙的两种溶液中溶质的质量分数相等 | |
| C. | t1℃时,将50g水加入15g甲物质中,可得到65g溶液 | |
| D. | 要使接近饱和的乙溶液转化为饱和溶液,可采用蒸发溶剂的方法 |


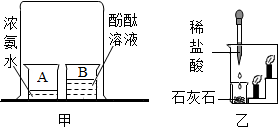 实验是进行科学探究的重要方式,请根据下图回答有关问题.
实验是进行科学探究的重要方式,请根据下图回答有关问题.