题目内容
14. 实验是进行科学探究的重要方式,请根据下图回答有关问题.
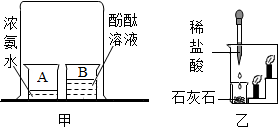
实验是进行科学探究的重要方式,请根据下图回答有关问题.(1)用甲图所示装置进行实验,可观察到的现象是B烧杯中酚酞溶液变红,A烧杯中无明显变化,这个实验说明氨水具有的性质是氨水具有挥发性(或碱性)(只填其中一点).
(2)用乙图所示装置探究二氧化碳性质时,小烧杯里发生反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,这个实验说明二氧化碳具有的性质是不能燃烧,也不支持燃烧,密度比空气大.
分析 根据已有的知识进行分析,分子在不断的运动,氨水呈碱性,能使酚酞试液变红;盐酸能与碳酸钙反应生成氯化钙、水和二氧化碳;二氧化碳不燃烧、不支持燃烧、密度比空气大,据此解答.
解答 解:(1)浓氨水具有挥发性,挥发出的氨分子不断的运动,溶于酚酞试液中使酚酞变红,故填:B烧杯中酚酞溶液变红,A烧杯中无明显变化 氨水具有挥发性(或碱性);
(2)盐酸能与碳酸钙反应生成氯化钙、水和二氧化碳;蜡烛由下而上依次熄灭,说明二氧化碳不能燃烧也不支持燃烧且密度比空气大,故填:
CaCO3+2HCl=CaCl2+H2O+CO2↑,二氧化碳不能燃烧也不支持燃烧,密度比空气大
故答案为:(1)B烧杯中酚酞溶液变红,A烧杯中无明显变化 氨水具有挥发性(或碱性)
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑ 不能燃烧,也不支持燃烧 密度比空气大
点评 本题考查了对化学实验的设计,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列化学用语的说法中不正确的是( )
| A. | 2个氮原子N2 | B. | 4个铝离子Al3+ | ||
| C. | 铁红的主要成分FeO | D. | 碳酸氢钠中的碳元素显+4价 |
3. 甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )| A. | t2℃时,向100g甲中加入100g水后形成溶液的质量为200g | |
| B. | t1℃时,甲、乙两种物质的溶解度相等 | |
| C. | 甲的溶解度比乙大 | |
| D. | 将t2℃时甲、乙的饱和溶液分别降到t1℃时,两溶液的溶质质量分数相等 |
4.节约资源,保护环境,倡导健康安全的生活理念,下列做法中,不合理的是( )
| A. | 使用降解塑料袋,减少“白色污染” | |
| B. | 将污水排入大明湖 | |
| C. | 察觉燃气泄漏后,严禁明火或电火花 | |
| D. | 将垃圾分类投放 |

 如图是水的电解实验装置图
如图是水的电解实验装置图


