题目内容
探究水蒸气通过灼热的木炭后,得到的混合气体的主要成分.
【提出猜想】该混合气体主要成分为CO、CO2、H2和H2O.
【查阅资料】a.浓硫酸可作干燥剂.b.氢气在加热的条件下与氧化铜反应生成铜和水.
【实验过程】设计实验装置如下:(部分夹持仪器已略去;假设每个装置里的药品足量,反应充分).
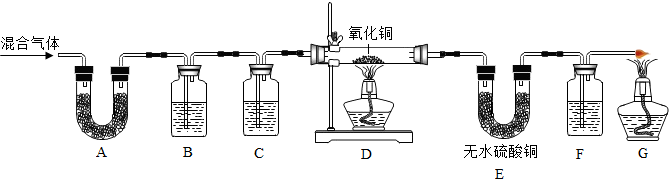
装置A中无水硫酸铜变蓝,写出该反应的化学方程式 ,装置B中澄清石灰水变浑浊,写出该反应的化学方程式 ,由此得出混合气体中含有CO2和H2O气体; ②通过观察装置D、E中的现象后,为了确认混合气体中含有氢气,装置C中的试剂是 .为了证明CO气体的存在,装置F中试剂是 .
【实验结论】猜想正确.
【提出猜想】该混合气体主要成分为CO、CO2、H2和H2O.
【查阅资料】a.浓硫酸可作干燥剂.b.氢气在加热的条件下与氧化铜反应生成铜和水.
【实验过程】设计实验装置如下:(部分夹持仪器已略去;假设每个装置里的药品足量,反应充分).

装置A中无水硫酸铜变蓝,写出该反应的化学方程式
【实验结论】猜想正确.
考点:常见气体的检验与除杂方法,书写化学方程式、文字表达式、电离方程式
专题:综合实验题
分析:根据无水硫酸铜遇水变蓝和澄清石灰水遇二氧化碳变浑浊,判断混合气体中的气体;并写出石灰水与二氧化碳的方程式;C装置应是除去水蒸气防止对氢气反应产生水的干扰进行分析.
(3)根据E中氧化铜变红、F中无水硫酸铜变蓝、G中澄清石灰水变浑浊,判断混合气体中其余气体;
(3)根据E中氧化铜变红、F中无水硫酸铜变蓝、G中澄清石灰水变浑浊,判断混合气体中其余气体;
解答:解:无水硫酸铜遇水变蓝,是硫酸铜和水反应产生五水硫酸铜,反应的方程式为:CuSO4+5H2O=CuSO4?5H2O;装置B中澄清石灰水变浑浊,是二氧化碳和氢氧化钙反应产生碳酸钙沉淀和水,反应的方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;C装置应是除去水蒸气防止对氢气反应产生水的干扰,因此盛放的是浓硫酸;因为一氧化碳还原氧化铜得到铜和二氧化碳,检验二氧化碳用澄清的石灰水,因此为了证明CO气体的存在,F中是澄清的石灰水.
故答案为:CuSO4+5H2O=CuSO4?5H2O;CO2+Ca(OH)2=CaCO3↓+H2O;浓硫酸;澄清石灰水.
故答案为:CuSO4+5H2O=CuSO4?5H2O;CO2+Ca(OH)2=CaCO3↓+H2O;浓硫酸;澄清石灰水.
点评:本题以实验探究的形式考查常见气体氢气、一氧化碳、二氧化碳和水蒸气的性质,同学们要具有综合的化学知识才能做好此题.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
以下反应的化学方程式书写正确的是( )
A、4Fe+3O2
| ||
| B、CaO+H2O→Ca(OH)2 | ||
C、2H2+O2
| ||
D、Ca(HCO3)2
|
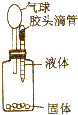 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )①锌和稀硫酸;②石灰石和盐酸;③氯化钠和水;④氧化钙和水.
| A、①② | B、①②④ |
| C、①④ | D、①③④ |
下列净水方法中,可以降低水的硬度的是( )
| A、过滤 | B、煮沸 | C、沉降 | D、吸附 |
属于分解反应的是( )
| A、Fe+CuSO4→FeSO4+Cu | ||
B、2H2O2
| ||
| C、CaO+H2O→Ca(OH)2 | ||
| D、NaOH+HCl→NaCl+H2O |
从化学的视角认识世界,下列对事实解释错误的是( )
| A、食物腐败:分子发生了变化 |
| B、热胀冷缩:分子大小随温度的变化而改变 |
| C、花香四溢:分子不停地运动 |
| D、H2和O2的性质不同:构成它们的分子不同 |
下列各组物质在溶液中能够大量共存的是( )
| A、BaCl2 NaCl H2SO4 |
| B、H2SO4 NaCl Na2CO3 |
| C、Na2SO4 KNO3 NaOH |
| D、NaOH H2SO4 HCl |
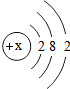 为某元素的原子结构示意图,x=
为某元素的原子结构示意图,x=