题目内容
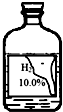 小琪和小思在探究酸与金属氧化物反应时选用如图溶液与CuO反应,发现产生大量气泡.
小琪和小思在探究酸与金属氧化物反应时选用如图溶液与CuO反应,发现产生大量气泡.【提出问题】为什么会有气泡产生?
【讨 论】该溶液不可能是稀H2SO4,有可能是H2O2.
【进行实验】向盛有少量二氧化锰的试管中加入少量该溶液,并迅速伸入带火星的木条,发现
带火星的木炭复燃
带火星的木炭复燃
,则该溶液是H2O2.【提出新问题】CuO是与H2O2反应还是作H2O2分解的催化剂?
【设计并进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取A、B两支试管,在A试管中加入1g的CuO,然后分别加入10mL的上述溶液,观察现象 | A试管中产生大量的气泡,B试管中无明显变化 A试管中产生大量的气泡,B试管中无明显变化 |
CuO是 H2O2分解的催化剂 |
| ②将该A试管中反应后的剩余物进行过滤、洗涤、烘干,称量 | 称得黑色滤渣质量为 1 1 g | |
| ③将步骤②中所得黑色滤渣取少量于试管中,并加入足量的稀H2SO4,观察现象 | 黑色粉末逐渐溶解,溶液由无色变为蓝色 黑色粉末逐渐溶解,溶液由无色变为蓝色 |
探究氧化铜的化学性质在反应前后是否发生改变
探究氧化铜的化学性质在反应前后是否发生改变
.【实验拓展】小琪认为针对该实验还有许多有价值的问题值得探究,请你帮他提出一点:
CuO和MnO2哪个对H2O2分解的催化效果更好(合理答案均可)
CuO和MnO2哪个对H2O2分解的催化效果更好(合理答案均可)
.分析:根据催化剂的特征进行分析,催化剂在化学反应前后的质量和化学性质都不变,改变的是化学反应的速率;检验氧气用带火星的木条;氧化铜能与硫酸反应生成硫酸铜和水.
解答:解:进行实验:双氧水和二氧化锰能产生氧气,而检验氧气用带火星的木条,木条复燃说明是氧气;
设计并进行实验:①在A试管中加入1g的CuO,然后分别加入等质量的10毫升H2O2溶液,目的是通过对比实验验证氧化铜能否加快过氧化氢的分解速率,根据结论可预测现象为A试管中产生大量的气泡,B试管中无明显变化;
②根据结论CuO是H2O2分解的催化剂可知,其质量在反应前后不变,故为1克;
③根据结论CuO是H2O2分解的催化剂可知,氧化铜在反应前后化学性质不变,又因为氧化铜能与硫酸反应生成硫酸铜和水,硫酸铜的水溶液为蓝色,故可以用于探究氧化铜的化学性质在反应前后是否发生改变.故填:黑色粉末逐渐溶解,溶液由无色变为蓝色;探究氧化铜的化学性质在反应前后是否发生改变;
实验拓展:要求提出的问题要有价值,如:CuO和MnO2哪个对H2O2分解的催化效果更好(合理答案均可)
故答案为:带火星的木炭复燃;A试管中产生大量的气泡,B试管中无明显变化;1;黑色粉末逐渐溶解,溶液由无色变为蓝色;探究氧化铜的化学性质在反应前后是否发生改变;CuO和MnO2哪个对H2O2分解的催化效果更好(合理答案均可).
设计并进行实验:①在A试管中加入1g的CuO,然后分别加入等质量的10毫升H2O2溶液,目的是通过对比实验验证氧化铜能否加快过氧化氢的分解速率,根据结论可预测现象为A试管中产生大量的气泡,B试管中无明显变化;
②根据结论CuO是H2O2分解的催化剂可知,其质量在反应前后不变,故为1克;
③根据结论CuO是H2O2分解的催化剂可知,氧化铜在反应前后化学性质不变,又因为氧化铜能与硫酸反应生成硫酸铜和水,硫酸铜的水溶液为蓝色,故可以用于探究氧化铜的化学性质在反应前后是否发生改变.故填:黑色粉末逐渐溶解,溶液由无色变为蓝色;探究氧化铜的化学性质在反应前后是否发生改变;
实验拓展:要求提出的问题要有价值,如:CuO和MnO2哪个对H2O2分解的催化效果更好(合理答案均可)
故答案为:带火星的木炭复燃;A试管中产生大量的气泡,B试管中无明显变化;1;黑色粉末逐渐溶解,溶液由无色变为蓝色;探究氧化铜的化学性质在反应前后是否发生改变;CuO和MnO2哪个对H2O2分解的催化效果更好(合理答案均可).
点评:本题考查了催化剂的特征运用,完成此题,可以依据催化剂的概念以及性质进行.注意语言表达要准确.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
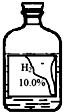 小琪和小思在探究酸与金属氧化物反应时选用如图溶液与CuO反应,发现产生大量气泡.
小琪和小思在探究酸与金属氧化物反应时选用如图溶液与CuO反应,发现产生大量气泡.
【提出问题】为什么会有气泡产生?
【讨 论】该溶液不可能是稀H2SO4,有可能是H2O2.
【进行实验】向盛有少量二氧化锰的试管中加入少量该溶液,并迅速伸入带火星的木条,发现________,则该溶液是H2O2.
【提出新问题】CuO是与H2O2反应还是作H2O2分解的催化剂?
【设计并进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取A、B两支试管,在A试管中加入1g的CuO,然后分别加入10mL的上述溶液,观察现象 | ________ | CuO是 H2O2分解的催化剂 |
| ②将该A试管中反应后的剩余物进行过滤、洗涤、烘干,称量 | 称得黑色滤渣质量为________g | |
| ③将步骤②中所得黑色滤渣取少量于试管中,并加入足量的稀H2SO4,观察现象 | ________ |
【实验拓展】小琪认为针对该实验还有许多有价值的问题值得探究,请你帮他提出一点:________.
小琪和小思在探究酸与金属氧化物反应时选用如图溶液与CuO反应,发现产生大量气泡.
【提出问题】为什么会有气泡产生?
【讨 论】该溶液不可能是稀H2SO4,有可能是H2O2.
【进行实验】向盛有少量二氧化锰的试管中加入少量该溶液,并迅速伸入带火星的木条,发现 ,则该溶液是H2O2.
【提出新问题】CuO是与H2O2反应还是作H2O2分解的催化剂?
【设计并进行实验】
【实验分析】上述实验步骤③的实验目的是 .
【实验拓展】小琪认为针对该实验还有许多有价值的问题值得探究,请你帮他提出一点: .
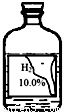
【提出问题】为什么会有气泡产生?
【讨 论】该溶液不可能是稀H2SO4,有可能是H2O2.
【进行实验】向盛有少量二氧化锰的试管中加入少量该溶液,并迅速伸入带火星的木条,发现 ,则该溶液是H2O2.
【提出新问题】CuO是与H2O2反应还是作H2O2分解的催化剂?
【设计并进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取A、B两支试管,在A试管中加入1g的CuO,然后分别加入10mL的上述溶液,观察现象 | CuO是 H2O2分解的催化剂 | |
| ②将该A试管中反应后的剩余物进行过滤、洗涤、烘干,称量 | 称得黑色滤渣质量为 g | |
| ③将步骤②中所得黑色滤渣取少量于试管中,并加入足量的稀H2SO4,观察现象 |
【实验拓展】小琪认为针对该实验还有许多有价值的问题值得探究,请你帮他提出一点: .

小琪和小思在探究酸与金属氧化物反应时选用如图溶液与CuO反应,发现产生大量气泡.
【提出问题】为什么会有气泡产生?
【讨 论】该溶液不可能是稀H2SO4,有可能是H2O2.
【进行实验】向盛有少量二氧化锰的试管中加入少量该溶液,并迅速伸入带火星的木条,发现 ,则该溶液是H2O2.
【提出新问题】CuO是与H2O2反应还是作H2O2分解的催化剂?
【设计并进行实验】
【实验分析】上述实验步骤③的实验目的是 .
【实验拓展】小琪认为针对该实验还有许多有价值的问题值得探究,请你帮他提出一点: .
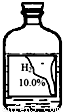
【提出问题】为什么会有气泡产生?
【讨 论】该溶液不可能是稀H2SO4,有可能是H2O2.
【进行实验】向盛有少量二氧化锰的试管中加入少量该溶液,并迅速伸入带火星的木条,发现 ,则该溶液是H2O2.
【提出新问题】CuO是与H2O2反应还是作H2O2分解的催化剂?
【设计并进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取A、B两支试管,在A试管中加入1g的CuO,然后分别加入10mL的上述溶液,观察现象 | CuO是 H2O2分解的催化剂 | |
| ②将该A试管中反应后的剩余物进行过滤、洗涤、烘干,称量 | 称得黑色滤渣质量为 g | |
| ③将步骤②中所得黑色滤渣取少量于试管中,并加入足量的稀H2SO4,观察现象 |
【实验拓展】小琪认为针对该实验还有许多有价值的问题值得探究,请你帮他提出一点: .
