题目内容
15.将铁粉和铜粉的混合物10g,放入100g的稀盐酸中,恰好完全反应.此时烧杯内各物质的总质量为109.8g.请计算:(1)根据质量守恒定律,计算反应后生成氢气的质量0.2g.
(2)计算混合物中含铜的质量.
(3)原稀盐酸中溶质的质量分数.
分析 根据铜不能和稀盐酸反应,铁和稀盐酸反应生成硫酸亚铁和氢气;
(1)铁与稀盐酸反应生成氯化亚铁,同时放出氢气;根据质量守恒定律,实验前后烧杯中物质的质量差即为反应放出氢气的质量;
(2)而利用铁和稀盐酸反应的方程式依据氢气的质量可以求出反应的铁的质量,进一步可以计算铜的质量进行解答;
(3)根据氢气的质量求出所用稀盐酸中溶质的质量,进而求出所用稀盐酸中溶质的质量分数即可.
解答 解:(1)反应后生成氢气的质量为:10g+100g-109.8g=0.2g,
(2)设铁的质量为x,所用稀盐酸中溶质的质量为y.
Fe+2HCl═FeCl2+H2↑
56 73 2
x y 0.2g
$\frac{56}{x}=\frac{73}{y}=\frac{2}{0.2g}$
x=5.6g
y=7.3g
混合物中含铜的质量=10g-5.6g=4.4g;
原稀盐酸中溶质的质量分数=$\frac{7.3g}{100g}×$100%=7.3%
答案:
(1)0.2g;
(2)混合物中含铜的质量4.4g;
(3)原稀盐酸中溶质的质量分数为7.3%.
点评 铜不能和稀盐酸反应,不能根据化学方程式进行计算,但是铁能和稀盐酸反应,根据化学方程式可以计算铁质量,从而可以计算铜的质量,要注意理解.

练习册系列答案
相关题目
18.下列物质能大量共存于水溶液中的是( )
| A. | HNO3 Ca(OH)2 NaCl | B. | KNO3 CuCl2 Na2SO4 | ||
| C. | NaOH MgSO4 BaCl2 | D. | HCl Na2CO3 Ca(NO3)2 |
6. 某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
【提出猜想】红色粉末可能是:①Cu ②Fe2O3 ③Cu和Fe2O3
【查阅资料】(1)白色无水CuSO4遇水变蓝
(2)Cu在FeCl3溶液中发生反应:2FeCl3+Cu═2FeCl2+CuCl2
【实验探究】
[甲组同学]:定性检测该红色粉末的物质组成
(1)小云取少量红色粉末于试管中,滴加足量稀盐酸,充分振荡后观察,发现固体全部溶解,得有色溶液.则猜想猜想①一定不成立一定不成立,其中一定发生反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.
(2)小伟向小云得到的有色溶液中插入一根洁净的铁丝,反应充分后,观察到铁丝表面有红色物质生成
现象,得出猜想③成立.
[乙组同学]:定量测定该红色粉末中氧化铁的质量分数
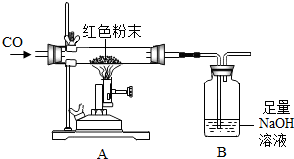
实验步骤:小晨称取该红色粉末5.0g装入硬质玻璃管中,按如图进行实验.开始时缓缓通入CO气体,过一段时间后再高温加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关物质的总质量(装置内空气中的水蒸气、CO2忽略不计),其数据如下表:
【交流讨论】
(1)在装置A中先通CO气体的目的是排尽玻璃管内的空气.A装置中发生反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)根据上述表格中的实验数据计算:红色粉末中氧化铁的质量分数为80%.
(3)从环保角度看上述装置有严重不足之处.你认为应该如何改进?缺少尾气处理装置;可以在导管口放点燃酒精灯,将一氧化碳烧掉.
【拓展延伸】对实验后B装置洗气瓶内溶液中是否有NaOH 剩余做进一步探究
实验步骤:小渊同学取该洗气瓶内溶液50克,逐滴加入质量分数为7.3%的稀盐酸至无气泡冒出为止,共用去稀盐酸60克,所得溶液质量为107.8克.试通过计算说明实验后B装置洗气瓶内溶液中是否有NaOH?(写出计算过程).
 某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.【提出猜想】红色粉末可能是:①Cu ②Fe2O3 ③Cu和Fe2O3
【查阅资料】(1)白色无水CuSO4遇水变蓝
(2)Cu在FeCl3溶液中发生反应:2FeCl3+Cu═2FeCl2+CuCl2
【实验探究】
[甲组同学]:定性检测该红色粉末的物质组成
(1)小云取少量红色粉末于试管中,滴加足量稀盐酸,充分振荡后观察,发现固体全部溶解,得有色溶液.则猜想猜想①一定不成立一定不成立,其中一定发生反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.
(2)小伟向小云得到的有色溶液中插入一根洁净的铁丝,反应充分后,观察到铁丝表面有红色物质生成
现象,得出猜想③成立.
[乙组同学]:定量测定该红色粉末中氧化铁的质量分数
实验步骤:小晨称取该红色粉末5.0g装入硬质玻璃管中,按如图进行实验.开始时缓缓通入CO气体,过一段时间后再高温加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关物质的总质量(装置内空气中的水蒸气、CO2忽略不计),其数据如下表:
| 反应前 | 反应后 | |
| Ⅰ 组 | 玻璃管和红色粉末的总质量为48.3g | 玻璃管和固体物质的总质量为47.1g |
| Ⅱ 组 | 洗气瓶和瓶中所盛物质的总质量为258.6g | 洗气瓶和瓶中所盛物质的总质量为261.91g |
(1)在装置A中先通CO气体的目的是排尽玻璃管内的空气.A装置中发生反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)根据上述表格中的实验数据计算:红色粉末中氧化铁的质量分数为80%.
(3)从环保角度看上述装置有严重不足之处.你认为应该如何改进?缺少尾气处理装置;可以在导管口放点燃酒精灯,将一氧化碳烧掉.
【拓展延伸】对实验后B装置洗气瓶内溶液中是否有NaOH 剩余做进一步探究
实验步骤:小渊同学取该洗气瓶内溶液50克,逐滴加入质量分数为7.3%的稀盐酸至无气泡冒出为止,共用去稀盐酸60克,所得溶液质量为107.8克.试通过计算说明实验后B装置洗气瓶内溶液中是否有NaOH?(写出计算过程).
7.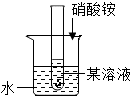 如图试管中盛放的是室温时的硝酸钾、氯化钠、熟石灰的饱和溶液中的一种,现向烧杯内加入硝酸铵晶体,试管中立即有大量的晶体析出,则试管中盛放的溶液的溶质是( )
如图试管中盛放的是室温时的硝酸钾、氯化钠、熟石灰的饱和溶液中的一种,现向烧杯内加入硝酸铵晶体,试管中立即有大量的晶体析出,则试管中盛放的溶液的溶质是( )
 如图试管中盛放的是室温时的硝酸钾、氯化钠、熟石灰的饱和溶液中的一种,现向烧杯内加入硝酸铵晶体,试管中立即有大量的晶体析出,则试管中盛放的溶液的溶质是( )
如图试管中盛放的是室温时的硝酸钾、氯化钠、熟石灰的饱和溶液中的一种,现向烧杯内加入硝酸铵晶体,试管中立即有大量的晶体析出,则试管中盛放的溶液的溶质是( )| A. | 硝酸钾 | B. | 氯化钠 | C. | 氯化氢 | D. | 熟石灰 |
4.生石灰是一种传统的建筑材料,俗称“石灰”.工业上通过在石灰窑中煅烧石灰石制得“石灰”,其反应原理是:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.兴趣小组的同学对某地刚出窑的“石灰”的成分进行探究.
【提出问题】刚出窑的“石灰”有那些成分?
【猜想】Ⅰ.只有氧化钙Ⅱ.只有碳酸钙Ⅲ.既有氧化钙也有碳酸钙
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅱ成立.乙同学认为上述实验不足以证明猜想Ⅱ成立,其理由是沉淀也可能是未溶解的氢氧化钙.
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是滴加的稀盐酸不足量.
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成他的实验报告.
【思考】使用“石灰”的建筑工地上常有一个大的石灰池,使用“石灰”时,先将生石灰倒入池内水中,一段时间后,再取用其中的石灰浆使用.长期使用的石灰池内壁会逐渐增厚,其主要原因是氢氧化钙吸收空气中的二氧化碳形成难溶的碳酸钙.
【提出问题】刚出窑的“石灰”有那些成分?
【猜想】Ⅰ.只有氧化钙Ⅱ.只有碳酸钙Ⅲ.既有氧化钙也有碳酸钙
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅱ成立.乙同学认为上述实验不足以证明猜想Ⅱ成立,其理由是沉淀也可能是未溶解的氢氧化钙.
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是滴加的稀盐酸不足量.
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成他的实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量剩余固体于试管中,加水振荡,过滤 取滤液滴加无色酚酞溶液 ②取样品滴加稀盐酸 | 溶液变红 有气泡产生 | 猜想Ⅲ成立 |
5.下列有关环境和能源的说法中,错误的是( )
| A. | 生活污水应集中处理达标后排放 | |
| B. | 煤、石油、天然气都属于不可再生能源,都是纯净物 | |
| C. | 使用乙醇汽油可以节省石油资源,减少汽车尾气污染环境 | |
| D. | 二氧化碳含量增大会使温室效应加剧,但是它不属于空气污染物 |
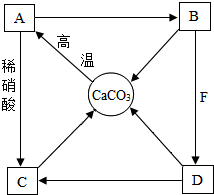 A~F是初中化学常见物质,A、B、C、D和CaCO3均含有同一种元素,其中B常用于改良酸性土壤,胃液中含有F.它们之间的转化关系如图所示,“→”表示相互转化.请回答:
A~F是初中化学常见物质,A、B、C、D和CaCO3均含有同一种元素,其中B常用于改良酸性土壤,胃液中含有F.它们之间的转化关系如图所示,“→”表示相互转化.请回答: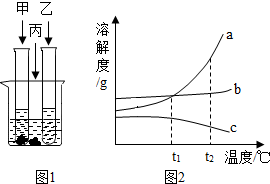 在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙还有剩余固体,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.
在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙还有剩余固体,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.