题目内容
9. 味精是我们烹调时常用的一种调味品,味精的主要成分是谷氨酸钠.在生产中味精按谷氨酸钠的含量多少被分为若干种规格.优质味精谷氨酸钠含量达99%以上,其余的则是用谷氨酸钠和不同量的精盐混制而成.某品牌味精包装上标注如图所示.某课外活动小组拟测定此味精中NaCl的含量是否符合其标注标准(谷氨酸钠的存在不影响NaCl的性质),按下列步骤进行实验:
味精是我们烹调时常用的一种调味品,味精的主要成分是谷氨酸钠.在生产中味精按谷氨酸钠的含量多少被分为若干种规格.优质味精谷氨酸钠含量达99%以上,其余的则是用谷氨酸钠和不同量的精盐混制而成.某品牌味精包装上标注如图所示.某课外活动小组拟测定此味精中NaCl的含量是否符合其标注标准(谷氨酸钠的存在不影响NaCl的性质),按下列步骤进行实验:①称取该味精样品10.0g;
②将样品加水溶解制成溶液;
③加入过量的硝酸银试剂,过滤;
④用蒸馏水反复洗涤沉淀多次;
⑤将沉淀小心烘干,称量,测得固体质量为2.87g;
⑥数据处理,经计算味精中NaCl的质量分数为11.7%
请根据上述实验步骤回答下列问题:
(1)步骤③中过滤操作所需要的仪器中除烧杯、铁架台(带铁圈)、玻璃棒外,还需要的仪器是漏斗.
(2)步骤②和步骤③都使用到玻璃棒,但它的目的不同,在步骤②的目的是加速溶解,在步骤③的目的是引流.
(3)步骤③中加入硝酸银试剂发生反应的化学方程式NaCl+AgNO3=NaNO3+AgCl↓.
(4)步骤③加入过量硝酸银试剂的目的是使氯化钠完全反应.
(5)从实验结果分析,该味精中NaCl的含量是否符合其包装袋上的标注标准不符合(填“符合”或“不符合”),理由是经计算味精中NaCl的质量分数为11.7%.
分析 (1)根据过滤需要的仪器进行分析;
(2)根据玻璃棒在溶解过程中的作用是加速溶解,在过滤时的作用时引流进行分析;
(3)根据氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠进行分析;
(4)根据硝酸银过量可以将氯化钠全部转化成沉淀进行分析;
(5)根据数据处理,经计算味精中NaCl的质量分数为11.7%进行分析.
解答 解:(1)过滤需要的仪器有:除烧杯、铁架台(带铁圈)、玻璃棒外,还需要的仪器是漏斗;
(2)玻璃棒在溶解过程中的作用是加速溶解,在过滤时的作用时引流;
(3)氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,化学方程式为:NaCl+AgNO3=NaNO3+AgCl↓;
(4)硝酸银过量可以将氯化钠全部转化成沉淀;
(5)经计算味精中NaCl的质量分数为11.7%,但是标签中氯化钠的含量是小于或等于10%,所以不符合标准.
故答案为:(1)漏斗;
(2)加速溶解,引流;
(3)NaCl+AgNO3=NaNO3+AgCl↓;
(4)使氯化钠完全反应;
(5)不符合,经计算味精中NaCl的质量分数为11.7%.
点评 进行解题是我们必须培养的能力,熟练的利用化学方程式根据已知的物质的质量计算求出其它物质的质量.

练习册系列答案
相关题目
20.小组同学查资料知道泡沫灭火器原理是:AlCl3+3NaHCO3=3NaCl+Al(OH)3↓+3CO2↑
【提出问题】此反应发生的原因是否由于AlCl3呈酸性?
【实验】测定AlCl3溶液的酸碱性
(1)用紫色石蕊试液测定溶液的酸碱性.
【提出问题】NH4Cl溶液呈酸性,它是否也能与NaHCO3溶液反应?
【实验】按如图进行实验:
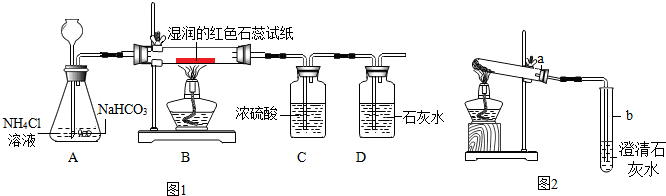
观察到的现象是:湿润的红色石蕊试纸变蓝,石灰水变浑浊
(2)说明生成的气体有NH3和CO2.
(3)C中浓硫酸吸收水蒸气和氨气
(4)A中的反应方程式是NaHCO3+NH4Cl=NaCl+NH3↑+CO2↑+H2O.
【实验反思】Ⅰ、Na2CO3和 NaHCO3的性质区别
按图2进行实验:取适量的NaHCO3粉末加到a试管中,加热,观察到a试管口有水生成,b试管中澄清石灰水变浑浊.持续加热直至两试管均不再发生变化时,发现a试管中仍残留有较多白色固体粉末.
(5)小文猜测白色固体粉末可能是:①NaOH;②Na2CO3;③NaCl.小燕认为猜想③一定不正确,理由是小苏打中不含氯元素,小燕从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,她判断该固体为NaOH,小美认为她的实验设计不合理,因为碳酸钠溶液也可以使酚酞变红.
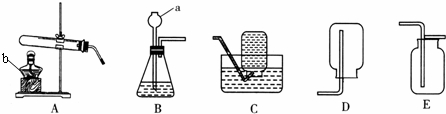
(6)他们继续探究固体成分,设计了如下实验:
通过实验证明:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+CO2↑+H2O,NaHCO3热稳定性较Na2CO3差.
【提出问题】此反应发生的原因是否由于AlCl3呈酸性?
【实验】测定AlCl3溶液的酸碱性
(1)用紫色石蕊试液测定溶液的酸碱性.
【提出问题】NH4Cl溶液呈酸性,它是否也能与NaHCO3溶液反应?
【实验】按如图进行实验:

观察到的现象是:湿润的红色石蕊试纸变蓝,石灰水变浑浊
(2)说明生成的气体有NH3和CO2.
(3)C中浓硫酸吸收水蒸气和氨气
(4)A中的反应方程式是NaHCO3+NH4Cl=NaCl+NH3↑+CO2↑+H2O.
【实验反思】Ⅰ、Na2CO3和 NaHCO3的性质区别
按图2进行实验:取适量的NaHCO3粉末加到a试管中,加热,观察到a试管口有水生成,b试管中澄清石灰水变浑浊.持续加热直至两试管均不再发生变化时,发现a试管中仍残留有较多白色固体粉末.
(5)小文猜测白色固体粉末可能是:①NaOH;②Na2CO3;③NaCl.小燕认为猜想③一定不正确,理由是小苏打中不含氯元素,小燕从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,她判断该固体为NaOH,小美认为她的实验设计不合理,因为碳酸钠溶液也可以使酚酞变红.
(6)他们继续探究固体成分,设计了如下实验:
| 操作步骤 | 实验现象 | 结论 |
| 取少量白色固体于试管中,加水溶解,向其中滴加足量氯化钙溶液 | 出现白色沉淀 | 剩余的固体有Na2CO3 |
| 静置,继续滴加酚酞 | 不变红 | 剩余的固体没有NaOH |

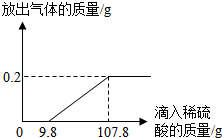 在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题:
在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题: