题目内容
1.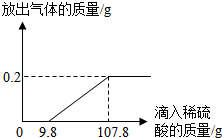 在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题:
在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题:(1)刚开始滴加稀硫酸没有氢气放出的原因是稀硫酸先和铝箔表面的氧化物反应.
(2)试计算所滴加的稀硫酸的溶质质量分数.(写出必要的计算过程,下同)
(3)滴入稀硫酸质量为107.8g时,所得溶液为不饱和溶液,试计算其溶质质量分数.
分析 铝能和空气中的氧气反应生成氧化铝;
氧化铝和稀硫酸反应生成硫酸铝和水;
铝和稀硫酸反应生成硫酸铝和氢气,根据氢气的质量可以计算反应的硫酸质量和生成的硫酸铝的质量,进一步可以计算所滴加的稀硫酸的溶质质量分数和所得溶液的溶质质量分数.
解答 解:(1)因为铝箔的表面有一层氧化铝,稀硫酸和氧化铝反应生成硫酸铝和水,不能产生氢气,因此刚开始滴加稀硫酸没有氢气放出.
故填:稀硫酸先和铝箔表面的氧化物反应.
(2)设和铝反应的硫酸质量为x,生成硫酸铝质量为y,
2Al+3H2SO4═Al2(SO4)3+3H2↑,
294 342 6
x y 0.2g
$\frac{294}{x}$=$\frac{342}{y}$=$\frac{6}{0.2g}$,
x=9.8g,y=11.4g,
所滴加的稀硫酸的溶质质量分数为:$\frac{9.8g}{107.8g-9.8g}$×100%=10%,
答:所滴加的稀硫酸的溶质质量分数为10%.
(3)设氧化铝和9.8g稀硫酸反应生成的硫酸铝质量为z,
Al2O3+3H2SO4═Al2(SO4)3+3H2O,
294 342
9.8g×10% z
$\frac{294}{9.8g×10%}$=$\frac{342}{z}$,
z=1.14g,
滴入稀硫酸质量为107.8g时,所得溶液溶质质量分数为:$\frac{11.4g+1.14g}{2.14g+107.8g-0.2g}$×100%=11.4%,
答:滴入稀硫酸质量为107.8g时,所得溶液溶质质量分数为11.4%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析图中数据的能力,计算时要注意规范性和准确性.

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案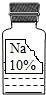 实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是A.
A.酸 B.碱 C.盐
【查阅资料】Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
Ⅱ.NaHCO3溶液呈碱性.
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
【作出猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl.
【设计并实验】
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得PH>7,这瓶试剂不可能是NaCl.
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 稀盐酸 | 产生大量的气泡 | 猜想②正确 相关的化学方程式Na2CO3+2HCl═2NaCl+CO2↑+H2O |
| 把产生的气体通入 澄清的石灰水 | 产生白色沉淀 | 相关的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O |
| A. | SiO2+4Mg $\frac{\underline{\;\;△\;\;}}{\;}$ 2MgO+Mg2Si | B. | Mg2Si+4HCl═2MgCl2+SiH4↑ | ||
| C. | 2Mg+O2$\frac{\underline{\;\;△\;\;}}{\;}$ 2MgO | D. | SiH4+2O2$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+2H2O |
| A. | 金属铜放入盐酸中,产生大量气泡 | |
| B. | 红磷在空气中燃烧时产生大量的白烟 | |
| C. | 点燃的铁丝在氧气中剧烈燃烧,火星四射 | |
| D. | 用冷的干燥小烧杯罩在蜡烛火焰上方,内壁出现水雾 |
 味精是我们烹调时常用的一种调味品,味精的主要成分是谷氨酸钠.在生产中味精按谷氨酸钠的含量多少被分为若干种规格.优质味精谷氨酸钠含量达99%以上,其余的则是用谷氨酸钠和不同量的精盐混制而成.某品牌味精包装上标注如图所示.某课外活动小组拟测定此味精中NaCl的含量是否符合其标注标准(谷氨酸钠的存在不影响NaCl的性质),按下列步骤进行实验:
味精是我们烹调时常用的一种调味品,味精的主要成分是谷氨酸钠.在生产中味精按谷氨酸钠的含量多少被分为若干种规格.优质味精谷氨酸钠含量达99%以上,其余的则是用谷氨酸钠和不同量的精盐混制而成.某品牌味精包装上标注如图所示.某课外活动小组拟测定此味精中NaCl的含量是否符合其标注标准(谷氨酸钠的存在不影响NaCl的性质),按下列步骤进行实验: