题目内容
2.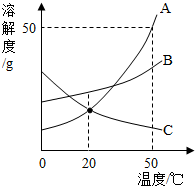 如图是A、B、C三种物质的溶解度曲线,下列分析正确的是( )
如图是A、B、C三种物质的溶解度曲线,下列分析正确的是( )| A. | 20℃时,三种物质的溶解度由大到小的顺序是B>A>C | |
| B. | 50℃时,A的饱和溶液的溶质质量分数是50% | |
| C. | 将50℃时100gA、B、C三种物质的饱和溶液降温到20℃,析出固体A最多 | |
| D. | 将20℃时三种物质的饱和溶液升高到50℃时,得到的都是饱和溶液 |
分析 A、据溶解度曲线可比较同一温度下不同物质的溶解度大小;
B、饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,并结合该温度下A的溶解度分析解答;
C、等质量的饱和溶液降低相同的温度,溶解度变化大的析出溶质多;
D、据物质的溶解度随温度变化分析溶液中溶质的变化情况,进而分析溶液状态转化.
解答 解:A、20℃时,三种物质的溶解度由大到小的顺序是B>A=C,故错误;
B、50℃时,A的溶解度是50g,所以饱和溶液的溶质质量分数是:$\frac{50g}{150g}$×100%<50%,故错误;
C、将50℃时100gA、B、C三种物质的饱和溶液降温到20℃,A的溶解度变化最大,析出固体最多,正确;
D、将20℃时三种物质的饱和溶液升高到50℃时,AB的溶解度变大,变为不饱和溶液,C的溶解度变小,析出溶质,仍然是饱和溶液,故错误;
故选:B.
点评 本题主要考查了饱和溶液中溶质的质量分数的计算方法、溶解度曲线的意义等知识,较好考查了学生对知识的掌握和应用.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
13.下列做法不利于环境保护的是( )
| A. | 废旧物品分类回收 | B. | 减少使用含磷洗衣粉 | ||
| C. | 减少农药和化肥的使用 | D. | 使用一次性塑料袋方便客户 |
10.某铜粉中混有少量铁粉,要将混合物中的铁粉除去,下列实验方案最合适的是( )
| A. | 混合物$→_{搅拌}^{足量稀硫酸}$过滤,洗涤,隔绝空气干燥 | |
| B. | 混合物$→_{搅拌}^{足量硫酸铜溶液}$ 过滤,洗涤,隔绝空气干燥 | |
| C. | 混合物 $→_{搅拌}^{足量硫酸锌溶液}$ 过滤,洗涤,隔绝空气干燥 | |
| D. | 混合物$→_{加强热}^{空气}$ 冷却$\stackrel{稀盐酸}{→}$过滤,洗涤,隔绝空气干燥 |
7.玻璃棒在化学实验中有着较广泛的用途,下列说法中不正确的是( )
| A. | 捣碎固体药品以加快其溶解速率 | |
| B. | 搅拌促进氢氧化钠溶液与盐酸充分反应 | |
| C. | 过滤时引流缓冲 | |
| D. | 蘸取溶液测定溶液的pH |

 称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液142g,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4↓+2NaCl)
称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液142g,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4↓+2NaCl) 如图是 A、B、C三种物质的溶解度曲线,回答下列问题:
如图是 A、B、C三种物质的溶解度曲线,回答下列问题: