题目内容
17.将8.0氧化铜固体放入100g稀硫酸中加热,恰好完全反应.试计算:(1)可生成硫酸铜16g
(2)所用稀硫酸的溶质质量分数是9.8%.
分析 氧化铜和稀硫酸反应生成硫酸铜和水,根据氧化铜的质量可以计算反应的硫酸的质量和生成的硫酸铜的质量,进一步可以计算稀硫酸中溶质的质量分数.
解答 解:(1)设稀硫酸中溶质的质量为x,生成的硫酸铜质量为y,
CuO+H2SO4═CuSO4+H2O,
80 98 160
8g x y
$\frac{80}{8g}=\frac{98}{x}=\frac{160}{y}$
x=9.8g,y=16g,
稀硫酸中溶质的质量分数为:$\frac{9.8g}{100g}$×100%=9.8%,
答案:
(1)16g
(2)9.8%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
5.下列反应属于分解反应的是( )
| A. | 食盐水→食盐+水 | B. | 氢气+氧气→水 | ||
| C. | 氯酸钾→氯化钾+氧气 | D. | 硫+氧气→二氧化硫 |
2.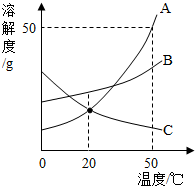 如图是A、B、C三种物质的溶解度曲线,下列分析正确的是( )
如图是A、B、C三种物质的溶解度曲线,下列分析正确的是( )
 如图是A、B、C三种物质的溶解度曲线,下列分析正确的是( )
如图是A、B、C三种物质的溶解度曲线,下列分析正确的是( )| A. | 20℃时,三种物质的溶解度由大到小的顺序是B>A>C | |
| B. | 50℃时,A的饱和溶液的溶质质量分数是50% | |
| C. | 将50℃时100gA、B、C三种物质的饱和溶液降温到20℃,析出固体A最多 | |
| D. | 将20℃时三种物质的饱和溶液升高到50℃时,得到的都是饱和溶液 |
13.物质的用途与性质密切相关,下列说法合理的是( )
| A. | 无水硫酸铜用于检验水份的存在 | |
| B. | 碱石灰用于干燥CO2气体 | |
| C. | Ca(OH)2可用于治疗缺钙症 | |
| D. | NaOH溶液能吸收污染空气的有害气体NO2、SO2和CO |
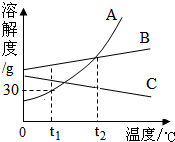 A、B、C三种不含结晶水的固体物质的溶解度曲线如图,回答有关问题.
A、B、C三种不含结晶水的固体物质的溶解度曲线如图,回答有关问题. 回答下列问题;
回答下列问题;