题目内容
10.利用下列仪器进行气体的制取和性质实验.请完成下列问题:
(1)写出下列仪器名称:A锥形瓶; D长颈漏斗;
(2)实验室用高锰酸钾制取并收集氧气,应选择的仪器是BCGHI(填编号);实验室用高锰酸钾制取制取氧气的化学反应方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室用盐酸和大理石制取并收集二氧化碳气体,可选择的仪器组合之一是ACDE(填编号),检验二氧化碳气体收集满的方法是将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;
(4)为变废为宝、节约能源、促进农村环境卫生,我省近年在农村大力推广沼气池建设项目.沼气的主要成份是甲烷(CH4),甲烷是没有颜色、没有气味的气体,比空气轻,是极难溶于水的可燃性气体.实验室常用无水醋酸钠和碱石灰固体混合加热来制取甲烷,如果用上述方法制取甲烷,应选择的反应发生装置是BGI,收集装置是CH.
分析 锥形瓶是常用的反应容器,长颈漏斗方便加液体药品;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.实验室常用无水醋酸钠和碱石灰固体混合加热来制取甲烷,因此需要加热,用到的仪器有BGI;沼气的主要成份是甲烷(CH4),甲烷是没有颜色、没有气味的气体,比空气轻,是极难溶于水的可燃性气体,因此可以用排水法收集,仪器是CH.
解答 解:(1)锥形瓶是常用的反应容器,长颈漏斗方便加液体药品,故答案为:锥形瓶;长颈漏斗;
(2)如果用高锰酸钾制氧气就需要加热,用高锰酸钾制取并收集氧气,应选择的仪器是:BCGHI;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:BCGHI;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,因此可选择的仪器组合之一是ACDE;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;故答案为:ACDE;将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;
(4)实验室常用无水醋酸钠和碱石灰固体混合加热来制取甲烷,因此需要加热,用到的仪器有BGI;沼气的主要成份是甲烷(CH4),甲烷是没有颜色、没有气味的气体,比空气轻,是极难溶于水的可燃性气体,因此可以用排水法收集,仪器是CH;故答案为:BGI;CH;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
【查阅资料】
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液呈碱性 | 水溶液呈碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
实验一:探究两者水溶液酸碱性的差异
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变红色,但食用纯碱溶液中颜色更深,由此推测可能食用纯碱溶液碱性更强.小欢认为要比较两种溶液的碱性强弱,可直接用pH试纸进行测定.
实验二:比较两种物质的热稳定性
设计如图(1)装置:小试管套装在带有支管的大试管中,整套装置气密性好,其他装置略去.
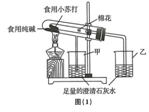 (1)为确保安全,实验结束时,在撤离酒精灯前必须完成的操作是把A、B试管中的导管移出液面.
(1)为确保安全,实验结束时,在撤离酒精灯前必须完成的操作是把A、B试管中的导管移出液面.(2)现象与结论:装有碳酸氢钠的试管口生成较多的无色小液滴,同时烧杯乙中有大量的气泡产生,澄清石灰水变浑浊;烧杯甲中也有气泡产生,澄清石灰水没有明显变化;实验结束后,经检验大、小两试管内的物质均是碳酸钠.结合以上实验,可得出结论:①碳酸氢钠受热生成的物质是碳酸钠、水和二氧化碳.②在受热条件下,碳酸钠比碳酸氢钠稳定.
实验三:比较与盐酸反应生成相同体积二氧化碳气体的快慢
取碳酸氢钠4.2g放入如图Ⅰ装置的锥形瓶中,取碳酸钠5.3g放入另一相同装置的锥形瓶中,分别加入相同质量、相同浓度的盐酸(足量).相同的条件下,通过图Ⅱ装置测量出生成气体的体积,得到时间-体积关系曲线如图Ⅲ所示.
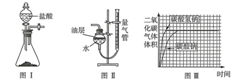
(4)已知二氧化碳不溶于该油层,图Ⅱ装置中油层的作用是防止部分的二氧化碳溶于水,造成实验误差.
(5)数据与分析:根据图Ⅲ曲线,可得出有关“比较与盐酸反应生成相同体积二氧化碳气体的快慢”的结论是在相同的条件下生成相同体积的二氧化碳,碳酸氢钠与盐酸反应比碳酸钠与盐酸反应快.
(6)反思与讨论:实验中“取碳酸氢钠4.2g、碳酸钠5.3g”的目的是生成相同体积的二氧化碳.
| A. | 原子是最小的粒子,不可再分 | |
| B. | 钠原子的质子数大于钠离子的质子数 | |
| C. | 分子、原子、离子都可以直接构成物质 | |
| D. | 当气态二氧化碳变成固态时,二氧化碳分子间不存在间隔 |
(1)提出问题:你提出的问题是:用酒精灯给物质加热时,应该用哪一层火焰?
(2)作出猜想:你的猜想是用酒精灯外焰给物质加热
(3)实验过程和记录:取出三支试管,各加入3mL的水.1、其中一支试管的底部放在火焰上方3cm处.2、将另一支试管的底部与灯芯接触加热.3、第三支试管的底部放在外焰部分加热.记录上述情况下将水加热至沸腾时所需时间如下:
| 情况1 | 情况2 | 情况3 | |
| 所需时间 | 87s | 54s | 25s |
| 结论 | |||
| A. | H2SO4 Na2O C CO | B. | Mg(OH)2 CuSO4 C CO2 | ||
| C. | KOH HNO3 O2 SO3 | D. | HCl NaOH O2 P2O5 |
| A. | 硫在空气中燃烧--明亮的蓝紫色火焰 | |
| B. | 铁丝在氧气中燃烧--火星四射,生成黑色固体 | |
| C. | 镁在氧气中燃烧--生成白色氧化镁固体 | |
| D. | 木炭在空气中燃烧--生成有刺激性气味的气体 |
 写出下列有关铁的现象及方程式
写出下列有关铁的现象及方程式