题目内容
20.NH4Al(SO4)2是食品加工行业中常用的添加剂,往往用于烘焙食品,下列有关该物质的说法错误的是( )| A. | 该物质由5种元素组成 | |
| B. | 该物质中NH4+和SO42-的微粒个数比为1:2 | |
| C. | 该物质中铝元素的化合价为+3价 | |
| D. | 该物质中氢元素和硫元素的质量比是1:8 |
分析 A.根据化学式的意义来分析;
B.根据物质的构成来分析;
C.根据化合物中元素化合价的计算方法来分析;
D.根据化合物中元素质量比的计算方法来分析.
解答 解:A.由NH4Al(SO4)2的化学式可知,它是由氮、氢、铝、硫、氧五种元素组成的,故正确;
B.由NH4Al(SO4)2的化学式可知,该物质中,NH4+和SO42-的微粒个数比为1:2,故正确;
C.在NH4Al(SO4)2中,铵根显+1价,硫酸根显-2价,化合物中各元素正负化合价的代数和为零,设其中铝元素的化合价为x,则(+1)+x+(-2)×2=0,则x=+3,故正确;
D.由NH4Al(SO4)2的化学式可知,该物质中,氢元素和硫元素的质量比为:(1×4):(32×2)=1:16,故错误.
故选D.
点评 本题考查了化学式的意义、根据化学式的计算、元素化合价的计算以及物质的结构,难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
11.下表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
(1)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取的方法有加入氢氧化钙(或升高温度)(写出一种即可)
(2)20℃时,191g 饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为19.1g.
(3)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶,过滤.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
(2)20℃时,191g 饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为19.1g.
(3)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶,过滤.
8. 如图是用比例模型来表示物质间发生化学变化的微观示意图,图中“●”、“○”分别表示两个不同元素的原子,能用该图示表示的化学反应是( )
如图是用比例模型来表示物质间发生化学变化的微观示意图,图中“●”、“○”分别表示两个不同元素的原子,能用该图示表示的化学反应是( )
 如图是用比例模型来表示物质间发生化学变化的微观示意图,图中“●”、“○”分别表示两个不同元素的原子,能用该图示表示的化学反应是( )
如图是用比例模型来表示物质间发生化学变化的微观示意图,图中“●”、“○”分别表示两个不同元素的原子,能用该图示表示的化学反应是( )| A. | H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl | B. | N2+3H2$\frac{\underline{\;催化剂\;}}{\;}$2NH3 | ||
| C. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | D. | N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO |
15.实验探究
氢气是一种密度比空气小、难溶于水的气体.实验室常用金属锌和硫酸溶液来制取少量氢气,反应的化学方程为:Zn+H2SO4═ZnSO4+H2↑.化学兴趣小组的同学根据实验室提供的仪器和药品,进行了如下探究实验.
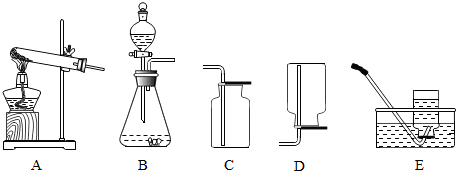
(1)制取氢气可选择图中的(填编号)B,选择此发生装置的理由是氢气的制取是固体和液体在常温下反应,若用此发生装置制取氧气,反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)小兵对“锌和硫酸反应快慢的影响因素”进行了探究.
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】
a.可能与硫酸溶液的浓度有关;
b.可能与锌的形状有关;
…
【设计并实验】小兵用不同浓度的硫酸溶液和不同形状的锌进行实验,记录如表所示.
对照实验是实验中只有一个变量,其他的量都保持不变.请你指出小兵实验中的对照实验(填实验编号)和变量(同种变量不重复得分).
第①组对照实验AC,变量硫酸的浓度(或质量分数);
第②组对照实验AB或CD,变量锌粒的形状.
【获得结论】
分析表中数据,可以得出的结论是硫酸的质量分数越大,反应速率越快;锌与硫酸的接触面积越大,反应速率越快;
【实验反思】
锌与硫酸溶液反应的快慢还可能受哪些因素影响?设计实验验证之.温度,取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间(只要有控制变量的意识即可).
氢气是一种密度比空气小、难溶于水的气体.实验室常用金属锌和硫酸溶液来制取少量氢气,反应的化学方程为:Zn+H2SO4═ZnSO4+H2↑.化学兴趣小组的同学根据实验室提供的仪器和药品,进行了如下探究实验.

(1)制取氢气可选择图中的(填编号)B,选择此发生装置的理由是氢气的制取是固体和液体在常温下反应,若用此发生装置制取氧气,反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)小兵对“锌和硫酸反应快慢的影响因素”进行了探究.
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】
a.可能与硫酸溶液的浓度有关;
b.可能与锌的形状有关;
…
【设计并实验】小兵用不同浓度的硫酸溶液和不同形状的锌进行实验,记录如表所示.
| 实验编号 | 硫酸溶液的浓度 (均取20mL) | 锌的形状 (均取1g) | 气体的体积(mL) (均收集3分钟) |
| A | 20% | 锌粒 | 31.7 |
| B | 20% | 锌片 | 50.9 |
| C | 30% | 锌粒 | 61.7 |
| D | 30% | 锌片 | 79.9 |
第①组对照实验AC,变量硫酸的浓度(或质量分数);
第②组对照实验AB或CD,变量锌粒的形状.
【获得结论】
分析表中数据,可以得出的结论是硫酸的质量分数越大,反应速率越快;锌与硫酸的接触面积越大,反应速率越快;
【实验反思】
锌与硫酸溶液反应的快慢还可能受哪些因素影响?设计实验验证之.温度,取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间(只要有控制变量的意识即可).
4.下列化学实验基本操作错误的是( )
| A. | 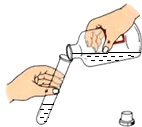 倾倒液体试剂 | B. | 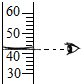 量取一定体积的液体 | ||
| C. | 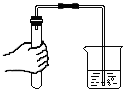 检查装置气密性 | D. | 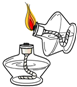 点燃酒精灯 |
5.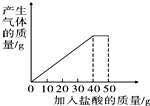 石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
请计算:
(1)石灰石样品中杂质的质量为4g;
(2)所加盐酸的溶质质量分数.
(3)当加入稀盐酸质量为40克时,所得溶液的质量为48.96克.
 石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 10 | 10 | 10 |
| 剩余固体的质量/g | 16 | 12 | 8 |
(1)石灰石样品中杂质的质量为4g;
(2)所加盐酸的溶质质量分数.
(3)当加入稀盐酸质量为40克时,所得溶液的质量为48.96克.