题目内容
14.回收利用是保护金属资源的一条有效途径.某工业废料含碱式碳酸铜【Cu2(OH)2CO3】和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,主要流程如下.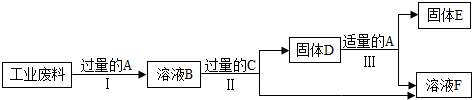
已知:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑ Fe+Fe2(SO4)3=3FeSO4
(1)过程Ⅰ中加入过量A的目的是使固体完全溶解.
(2)过程Ⅱ中发生的置换反应是Fe+CuSO4=FeSO4+Cu;Fe+H2SO4=FeSO4+H2↑,充分反应后,还应有的实验操作过滤.
(3)过程Ⅲ加入适量A的作用是除去铁,且使溶液F不引入杂质.
分析 (1)由题干信息可知,A是稀硫酸;
(2)加入过量的铁粉用以置换出铜;
(3)根据分离铁和铜的混合物来分析.
解答 解:(1)过程Ⅰ中加入过量稀硫酸的目的是使固体完全溶解;故填:使固体完全溶解;
(2)加入铁粉后,铁与硫酸铜反应生成铜和硫酸亚铁;铁与稀硫酸反应生成硫酸亚铁和氢气,这两个反应是置换反应;铁与硫酸铁反应生成硫酸亚铁,该反应是化合反应,过程Ⅱ充分反应后,要得到固体和溶液,需要经过过滤操作;故填:Fe+CuSO4=FeSO4+Cu;Fe+H2SO4=FeSO4+H2↑,过滤;
(3)加入适量的稀硫酸,加到不再产生气泡为止,其中的铁充分反映,故填:除去铁,且使溶液F不引入杂质.
点评 金属的性质是中考主要考点之一,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
4.推理是一种重要的学习方法.下列推理中正确的是( )
| A. | 酸和碱发生中和反应生成盐和水,则生成盐和水的化学反应一定是中和反应 | |
| B. | 酸性溶液能使紫色石蕊溶液变红,则能使紫色石蕊溶液变红的一定是酸性溶液 | |
| C. | 饱和溶液不能继续溶解某种溶质.则其它物质也不能继续溶解在该饱和溶液中 | |
| D. | 同种分子构成的物质一定是纯静物,则纯净物一定都是由同种分子构成的 |
5.锰丝放入稀硫酸中,有气泡产生,放入硫酸铝溶液中,表面没有金属析出.下列关于锰活动性判断不正确的是( )
| A. | Mn>Cu | B. | Al>Mn | C. | Mn>H | D. | Mn>Mg |
19.如图所示装置中,容器Ⅰ、II体积相同,U形管内左右两侧液面相平,且装置气密性良好.实验时,打开分液漏斗旋塞,将液体同时滴入容器,滴加完毕后关闭旋塞.
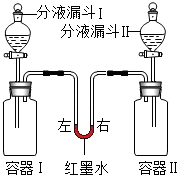
实验内容及相关现象如下表所示.
(1)实验A中,容器Ⅰ中的现象是石灰水变浑浊,容器Ⅱ中反应的化学方程式是H2O+CO2=H2CO3.
(2)实验B中,“①”的实验现象是右侧高左侧低,出现此现象的原因是等体积的氢氧化钠溶液比石灰水消耗的二氧化碳多.
(3)实验C中,依据盐酸浓度相同且足量,反应结束并恢复至室温后,红墨水液面位置计算出镁的质量为0.24g.

实验内容及相关现象如下表所示.
| 实验 编号 | 容器Ⅰ | 分液漏斗Ⅰ | 容器Ⅱ | 分液漏斗Ⅱ | 红墨水液面位置 |
| A | 二氧化碳 (充满) | 10mL澄清 石灰水 | 二氧化碳 (充满) | 10mL水 | 左侧高右侧低 |
| B | 二氧化碳 (充满) | 10mL澄清 石灰水 | 二氧化碳 (充满) | 10mL浓氢氧化钠溶液 | ① |
| C | 0.65g锌 | 10mL盐酸 | 镁 | 10mL盐酸 | 室温时恢复至起始状态 |
(2)实验B中,“①”的实验现象是右侧高左侧低,出现此现象的原因是等体积的氢氧化钠溶液比石灰水消耗的二氧化碳多.
(3)实验C中,依据盐酸浓度相同且足量,反应结束并恢复至室温后,红墨水液面位置计算出镁的质量为0.24g.
3.某同学用pH试纸测出日常生活中几种常见物质的pH,其中酸性最强的是( )
| A. | 肥皂水:pH=10 | B. | 酸奶:pH=4 | C. | 漂白液:pH=13 | D. | 洁厕精:pH=1 |
8.某化学兴趣小组为了探究铬与常见金属铝、铜在金属活动性顺序的相对位置关系,进行了如下探究活动:
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜.铬能与稀硫酸反应,生成氢气和硫酸铬(CrSO4).
【提出猜想】对这三种金属的活动性顺序提出了如下猜想:
猜想①:Cr>Al>Cu
猜想②:Cr>Cu>Al
猜想③:Al>Cr>Cu
猜想④:Al>Cu>Cr
【讨论交流】根据已学的金属活动性顺序和已查阅的资料分析,肯定不能成立的是猜想②④(填序号).
【实验设计及过程】请将表中的内容填写完整.
【实验反思】
(1)将金属片投入稀硫酸前应先打磨金属片的目的是除去金属表面氧化物,有利于直接反应.
(2)有同学提出探究金属活动性强弱还可以依据“金属与金属化合物溶液是否发生置换反应”来判断.为了验证甲、乙、丙三种金属的活动性依次减弱,某同学设计了如下方案:
①把甲放入乙的化合物溶液中;
②把乙放入丙的化合物溶液中;
③把甲放入丙的化合物溶液中;
你认为上述方案中的③(填序号)没有必要做.
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀的致密氧化膜.铬能与稀硫酸反应,生成氢气和硫酸铬(CrSO4).
【提出猜想】对这三种金属的活动性顺序提出了如下猜想:
猜想①:Cr>Al>Cu
猜想②:Cr>Cu>Al
猜想③:Al>Cr>Cu
猜想④:Al>Cu>Cr
【讨论交流】根据已学的金属活动性顺序和已查阅的资料分析,肯定不能成立的是猜想②④(填序号).
【实验设计及过程】请将表中的内容填写完整.
| 实验操作 | 实验现象 | 实验结论 |
| 室温下,将大小相同并打磨光亮的铬片、铝片、铜片分别浸入盛有体积相同、溶质质量分数相同的稀硫酸试管中 | 铬片表面产生气泡缓慢,铝片表面产生气泡较快,铜片表面无现象 | 猜想③(填序号)成立 |
(1)将金属片投入稀硫酸前应先打磨金属片的目的是除去金属表面氧化物,有利于直接反应.
(2)有同学提出探究金属活动性强弱还可以依据“金属与金属化合物溶液是否发生置换反应”来判断.为了验证甲、乙、丙三种金属的活动性依次减弱,某同学设计了如下方案:
①把甲放入乙的化合物溶液中;
②把乙放入丙的化合物溶液中;
③把甲放入丙的化合物溶液中;
你认为上述方案中的③(填序号)没有必要做.
