题目内容
15. 用“侯式联合制碱法”制得的纯碱含有少量的氯化钠,为测定某纯碱样品中碳酸钠的含量,取23g样品置于烧杯中,加水将其溶解,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示.求
用“侯式联合制碱法”制得的纯碱含有少量的氯化钠,为测定某纯碱样品中碳酸钠的含量,取23g样品置于烧杯中,加水将其溶解,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示.求(1)当滴入氯化钙溶液至图中B点时,烧杯中溶液里含有的溶质是(写化学式)NaCl、CaCl2;
(2)求该纯碱样品中碳酸钠的质量分数(精确到0.1%).
(3)当滴入氯化钙溶液至图中A点时,并且反应后烧杯中溶液为不饱和溶液,计算该溶液中溶质的质量.
分析 碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)当滴入氯化钙溶液至图中B点时氯化钙过量,因此烧杯中溶液里含有的溶质是NaCl、CaCl2.
故填:NaCl、CaCl2.
(2)设碳酸钠质量为x,生成氯化钠质量为y,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100 117
x 20g y
$\frac{106}{x}$=$\frac{100}{20g}$=$\frac{117}{y}$,
x=21.2g,y=23.4g,
该纯碱样品中碳酸钠的质量分数为:$\frac{21.2g}{23g}$×100%=92.2%,
答:该纯碱样品中碳酸钠的质量分数为92.2%.
(3)当滴入氯化钙溶液至图中A点时,反应后烧杯中溶液为不饱和溶液,该溶液中溶质的质量为:23g-21.2g+23.4g=25.2g,
答:该溶液中溶质的质量为25.2g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
7.如图图示实验操作中,正确的是( )
| A. | 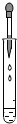 滴加液体 | B. |  往试管加入固体 | C. |  倾倒液体 | D. | 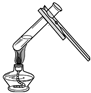 加热液体 |
4.下列各组物质中,必须利用化学性质的不同才能区别的是( )
| A. | 水和食醋 | B. | 铜片和铝片 | C. | 氧气和二氧化碳 | D. | 铁粉和食盐 |
 构成物质的粒子之间的关系如图所示.回答下列问题:
构成物质的粒子之间的关系如图所示.回答下列问题: 探究空气成分时在实验室中我们常用燃烧红磷(或白磷)的方法来“测定空气中氧气含量”(如图所示),其反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;实验测得氧气的含量小于21%,小明检查后发现气密性良好,经过分析我认为可能的原因是红磷量不足,若改用其它代用可燃物来代替红磷,在选择可燃物时,我认为必须考虑的因素是:
探究空气成分时在实验室中我们常用燃烧红磷(或白磷)的方法来“测定空气中氧气含量”(如图所示),其反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;实验测得氧气的含量小于21%,小明检查后发现气密性良好,经过分析我认为可能的原因是红磷量不足,若改用其它代用可燃物来代替红磷,在选择可燃物时,我认为必须考虑的因素是: